题目内容
20.通过一年的化学学习,同学们总结了一些知识如下:(1)服用含Al(OH)3的药物可治疗胃酸过多,其反应方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(2)家里洗碗时,餐具上的油污用加入洗洁精于水中更易洗净.
(3)金属与盐溶液之间的置换反应,一般是活动性较强的金属可把活动性较弱的金属从其盐溶液中置换出来,如铜和硝酸银溶液反应,其化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2,非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如有下列反应:C12+2NaBr=2NaCl+Br2; I2+Na2S=2NaI+S↓;Br2+2KI=2KBr+I2,由此可判断:S、C12、I2、Br2活动性由强到弱顺序是C12>Br2>I2>S.
分析 (1)根据氢氧化铝和盐酸反应生成氯化铝和水进行分析;
(2)根据洗洁精可以乳化油污进行分析;
(3)根据铜比银活泼,能和硝酸银反应生成硝酸铜和银,活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来进行分析.
解答 解:(1)氢氧化铝和盐酸反应生成氯化铝和水,化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O;
(2)洗洁精可以乳化油污,所以家里洗碗时,餐具上的油污用加入洗洁精于水中更易洗净;
(3)铜比银活泼,能和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgNO3═2Ag+Cu(NO3)2,由C12+2NaBr=2NaCl+Br2;I2+Na2S=2NaI+S↓;Br2+2KI=2KBr+I2可以判断出S、C12、I2、Br2活动性由强到弱的顺序是C12>Br2>I2>S.
故答案为:(1)Al(OH)3+3HCl═AlCl3+3H2O;
(2)洗洁精;
(3)Cu+2AgNO3═2Ag+Cu(NO3)2,C12>Br2>I2>S.
点评 解答本题要充分理解金属活动性顺序的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
10.下列物质中属于纯净物的是( )
| A. | 空气 | B. | 粗盐 | C. | 生铁 | D. | 熟石灰 |
11.物质的组成和结构决定物质的性质,下列解释合理的是( )
| A. | H2O与H2O2的化学性质不同的原因是原子个数不同 | |
| B. | 金刚石和石墨的物理性质差异大的原因是碳原子个数不同 | |
| C. | 生铁与钢的性能不同的原因是含碳量不同 | |
| D. | 稀盐酸与稀硫酸的化学性质相似的原因是都含有酸根离子 |
15.某同学对所学的部分化学知识归纳如下,其中完全正确的一组是( )
| 化肥的种类、鉴别及使用 | 化学应用 | ||
A | CO(NH2)2、(NH4)2SO4和NaNO3均可用作氮肥 从外观上可区分硫酸钾和磷矿粉两种肥料 给农作物施肥时同时施用草木灰和碳酸氢铵以提高肥效 | B | 用肥皂水检验硬水和软水 用食醋清洗家用瓷器上的水垢 用燃烧后闻气味的方法鉴别衣服面料是蚕丝还是合成纤维涤纶 |
| 食品安全 | 能源与环境 | ||
C | 用硫磺熏制白木耳、粉丝等食品 用小苏打作焙制糕点的发酵粉 除鱼胆汁苦味(酸性)--纯碱溶液浸泡 | D | 煤、石油燃烧--无污染 车用乙醇汽油--减少污染 氢能--无污染 |
| A. | A | B. | B | C. | C | D. | D |
7.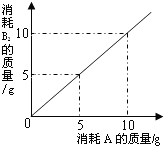 在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
 在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )| A. | 10g | B. | 13g | C. | 16g | D. | 18g |
4.下列反应属于分解反应的是( )
| A. | 乙炔+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| B. | 红磷+氧气$\stackrel{点燃}{→}$五氧化二磷 | |
| C. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 | |
| D. | 分离液态空气得氮气和氧气 |
5.能源、资源、环境与人类的生活和社会的发展密切相关.
(1)石油、煤、天然气合称为三大化石燃料.
①煤燃烧时排放出SO2、NO2等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水会形成酸雨.
②2014年青奥会在南京举行,为了控制汽车尾气给空气造成的污染,我市在燃料的使用和管理等方面采取了一些有效措施,如节能环保车的使用,这也是未来的发展趋势.
图2是我国自行研制的氢动力概念跑车.汽车最理想的清洁燃料是氢气,但氢动力汽车目前还不能普及的原因是氢气制取成本高或贮存困难(只需写出一点).
(2)水是地球上最普通、最常见的物质之一.
①自来水厂净化水的步骤一般有加絮凝剂、沉淀、过滤、活性炭吸附、消毒剂消毒等步骤.检验自来水是否为硬水常用的物质是肥皂水.生活中通过煮沸的方法可以降低水的硬度.实验室配制氯化钠溶液应该用蒸馏水(填“自来水”或“蒸馏水”).
②从社会角度看:2014年3月22-28日是第二十七届“中国水周”.活动的宣传主题为“节约保护水资源,大力建设生态文明”.下列做法符合宣传主题的是AB.
A.富含氮、磷的生活污水不能排放到河中 B.农业浇灌推广使用喷灌、滴灌技术
C.不间断地放水洗衣服 D.工业污水直接压入地下
③新型自来水净水剂ClO2可由如下反应制取:Cl2+2X═2NaCl+2ClO2,X的化学式为NaClO2.
(3)人类每年都要从大自然中提取大量的金属,用于工农业生产和其他领域.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
①用下列试剂验证这三种金属的活动性顺序,能达到目的是B(填序号).
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
②某工厂的废液中含有硝酸银和硝酸铜,为回收资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,无气体产生.
下列说法正确的是A(选填字母).
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,一定没有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜
③常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图3实验探究铁粉与水蒸气反应后的产物.
a.试管尾部放一团湿棉花的目的是提供水蒸气.
b.探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
c.探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
④某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图4所示.所得溶液中所含溶质的化学式为Fe2(SO4)3、FeSO4,计算溶液中硫酸铁的质量.(要求写出计算过程)
(1)石油、煤、天然气合称为三大化石燃料.
①煤燃烧时排放出SO2、NO2等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水会形成酸雨.
②2014年青奥会在南京举行,为了控制汽车尾气给空气造成的污染,我市在燃料的使用和管理等方面采取了一些有效措施,如节能环保车的使用,这也是未来的发展趋势.

图2是我国自行研制的氢动力概念跑车.汽车最理想的清洁燃料是氢气,但氢动力汽车目前还不能普及的原因是氢气制取成本高或贮存困难(只需写出一点).
(2)水是地球上最普通、最常见的物质之一.
①自来水厂净化水的步骤一般有加絮凝剂、沉淀、过滤、活性炭吸附、消毒剂消毒等步骤.检验自来水是否为硬水常用的物质是肥皂水.生活中通过煮沸的方法可以降低水的硬度.实验室配制氯化钠溶液应该用蒸馏水(填“自来水”或“蒸馏水”).
②从社会角度看:2014年3月22-28日是第二十七届“中国水周”.活动的宣传主题为“节约保护水资源,大力建设生态文明”.下列做法符合宣传主题的是AB.
A.富含氮、磷的生活污水不能排放到河中 B.农业浇灌推广使用喷灌、滴灌技术
C.不间断地放水洗衣服 D.工业污水直接压入地下
③新型自来水净水剂ClO2可由如下反应制取:Cl2+2X═2NaCl+2ClO2,X的化学式为NaClO2.
(3)人类每年都要从大自然中提取大量的金属,用于工农业生产和其他领域.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.
①用下列试剂验证这三种金属的活动性顺序,能达到目的是B(填序号).
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
②某工厂的废液中含有硝酸银和硝酸铜,为回收资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,无气体产生.
下列说法正确的是A(选填字母).
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,一定没有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜
③常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如图3实验探究铁粉与水蒸气反应后的产物.
a.试管尾部放一团湿棉花的目的是提供水蒸气.
b.探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
c.探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
④某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅、锰等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图4所示.所得溶液中所含溶质的化学式为Fe2(SO4)3、FeSO4,计算溶液中硫酸铁的质量.(要求写出计算过程)
 ,则锂原子在化学反应中易失(填“得”或“失”)电子.
,则锂原子在化学反应中易失(填“得”或“失”)电子.