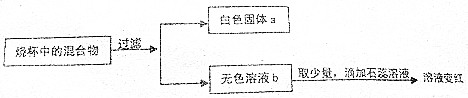
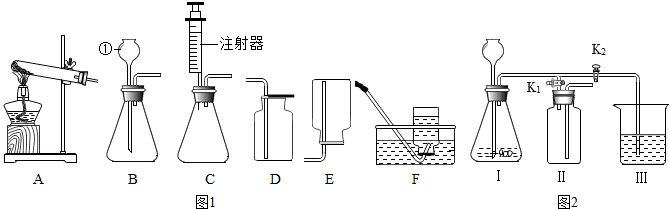
题目内容
3.已知A、E为黑色固体,F为红色固体,B、C、D常温下为气体(1)请写出下列物质的化学式:
AC;BO2;CCODCO2;ECuO;FCu
(2)请写出下列反应的化学方程式
①2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;②CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;③2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
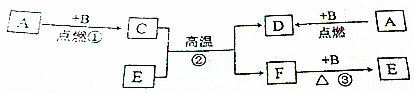
分析 根据A、E为黑色固体,F为红色固体,B、C、D常温下为气体,A和B点燃会生成D,所以A是碳,B是氧气,D就是二氧化碳,所以C是一氧化碳,一氧化碳和E高温会生成二氧化碳和F,所以E是氧化铜,F是铜,铜和氧气加热生成氧化铜,然后将推出的物质进行验证即可.
解答 解:(1)A、E为黑色固体,F为红色固体,B、C、D常温下为气体,A和B点燃会生成D,所以A是碳,B是氧气,D就是二氧化碳,所以C是一氧化碳,一氧化碳和E高温会生成二氧化碳和F,所以E是氧化铜,F是铜,铜和氧气加热生成氧化铜,经过验证,推导正确,所以A是C,B是O2,C是CO,D是CO2,E是CuO,F是Cu;
(2)①是碳和氧气点燃生成一氧化碳,化学方程式为:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;
②是一氧化碳和氧化铜加热生成铜和二氧化碳,化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
③是铜和氧气加热生成氧化铜,化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
故答案为:(1)C,O2,CO,CO2,CuO,Cu;
(2)2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.如表是NaCl和KNO3,在不同温度下的溶解度,下列说法中不正确的是( )
| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
| A. | 20℃时,NaCl溶解度大于KNO3的溶解度 | |
| B. | 两物质溶解度相等的温度在20~30℃之间 | |
| C. | 40℃时,向盛有5g NaCl的烧杯中加入10g水可得到溶质质量分数为33.3%的溶液 | |
| D. | 50℃时,向盛有10g KNO3的烧杯中加入20g水,充分溶解后再降温到30℃,有KNO3固体析出 |
13.某同学欲测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取60g该溶液于烧杯中,向其中滴入足量的氢氧化钠溶液,记录有关数据如表:
反应的化学方程式为:MgSO4+2NaOH═Na2SO4+Mg(OH)2
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
| 反应前 | 反应后 | |
| 烧杯和硫酸镁溶液的质量 | 溶质质量分数为10%的NaOH溶液 | 过滤后烧杯和溶液总质量 |
| 80g | 100g | 177.1g |
(1)反应生成氢氧化镁沉淀的质量为2.9g;
(2)计算MgSO4溶液中溶质的质量分数10%(根据化学方程式计算);
(3)100g溶质质量分数为10%的NaOH溶液中氧元素的质量为84g.
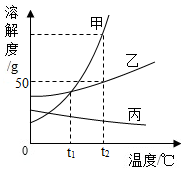 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题: 如图为我国某次盛大集会上黑龙江省参展的彩车“龙腾盛世”,请按要求回答下列问题:
如图为我国某次盛大集会上黑龙江省参展的彩车“龙腾盛世”,请按要求回答下列问题: