题目内容
小娟想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶末标明溶质质量分数的稀盐酸和必要的仪器。
(1)你认为她能测出铜的质量分数的合金是__________________合金。
(2)小娟取该合金的粉末32.5 g,与足量该盐酸充分反应后,经测定产 生了0.4 g气体,请你帮助她计算出该合金中铜的质量分数。
生了0.4 g气体,请你帮助她计算出该合金中铜的质量分数。
___Cu-Zn_____________合金。
(2)
.解设:参加反应的Zn的质量为x
Zn+2HCl=ZnCl2+H2↑
65 2
X 0、4g
65 2 32、5g-13g
—= — x=13g 该合金中铜的质量分数=___________X100%=60%
X  0、4g 32、5g
0、4g 32、5g
答:。。。。。。。。。。。。。。。。。

某同学对气体的实验室制法作以下探究,请根据图回答下列问题:
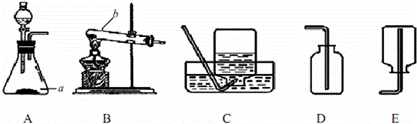 |
(1)写出标有序号的仪器的名称a ;b
(2)请写出能用B装置制取氧气的化学方程式 ;
(3)若发生装置选A,收集装置选C,则制取该气体的化学反应方程式为: 。
(4)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),氨气易溶于水。同时得到氯化钙和水。应选用的制取装置是
(填编号)选用的收集装置为 (填编号)
 D.化学反应中,原子总数随时间的变化
D.化学反应中,原子总数随时间的变化 下列
下列
 (1)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 。
(1)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 。
 ,
,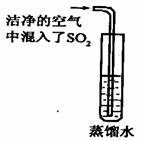 只要出现 的实验结果,
只要出现 的实验结果,