题目内容
铁是目前生产和使用量最大的金属.
(1)铁强化酱油中含有铁,此处的”铁“是指 (填”分子“、”原子“或”元素“).
(2)用一种溶液即可验证Zn、Fe、Cu三种金属的活动性顺序,这种溶液是 ,写出其中任意一个反应的化学方程式 .
(1)铁强化酱油中含有铁,此处的”铁“是指
(2)用一种溶液即可验证Zn、Fe、Cu三种金属的活动性顺序,这种溶液是
考点:金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据物质是由元素组成的解答;
(2)根据金属活动顺序进行思考,Ag、Fe、Cu这三种金属的金属活动性由强到弱的顺序为Fe>Cu>Ag.在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱.
(2)根据金属活动顺序进行思考,Ag、Fe、Cu这三种金属的金属活动性由强到弱的顺序为Fe>Cu>Ag.在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱.
解答:解:(1)物质是由元素组成的,铁强化酱油中含有铁,此处的”铁“是指铁元素,故答案:元素;
(2)Zn、Fe、Cu三种金属的活动性顺序是Zn>Fe>Cu,所以可选用活动性居中的铁的可溶性的盐进行探究如硫酸亚铁、氯化亚铁等;还可选用稀盐酸或稀硫酸,锌和铁都能反应但锌反应速度快,铁反应速度较慢,铜不反应;锌和硫酸亚铁反应生成硫酸锌和铁,反应的化学方程式为Zn+FeSO4=ZnSO4+Fe;故答案:硫酸亚铁(或硝酸亚铁、氯化亚铁或稀盐酸或稀硫酸);Zn+FeSO4=ZnSO4+Fe.
(2)Zn、Fe、Cu三种金属的活动性顺序是Zn>Fe>Cu,所以可选用活动性居中的铁的可溶性的盐进行探究如硫酸亚铁、氯化亚铁等;还可选用稀盐酸或稀硫酸,锌和铁都能反应但锌反应速度快,铁反应速度较慢,铜不反应;锌和硫酸亚铁反应生成硫酸锌和铁,反应的化学方程式为Zn+FeSO4=ZnSO4+Fe;故答案:硫酸亚铁(或硝酸亚铁、氯化亚铁或稀盐酸或稀硫酸);Zn+FeSO4=ZnSO4+Fe.
点评:要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.但也要注意,与金属反应酸一般是指稀硫酸和盐酸,不包括浓硫酸和硝酸.

练习册系列答案
相关题目
下列转化不能一步实现的是( )
| A、CO→CO2 |
| B、H2O→H2 |
| C、Ca(OH)2→NaOH |
| D、KNO3→KCl |

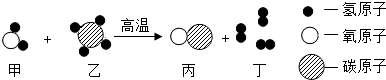
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子
”表示氧原子