题目内容
3.镁与盐酸反应的方程式为Mg+2HCl═MgCl2+H2↑,2.4克镁与50克盐酸恰好完全反应,则生成氢气的质量是( )| A. | 0.2g | B. | 0.02g | C. | 2g | D. | 20g |
分析 由金属镁的质量根据镁与稀盐酸反应的化学方程式可以计算出生成氢气的质量.
解答 解:设生成氢气的质量为x
Mg+2HCl═MgCl2+H2↑
24 2
2.4g x
$\frac{24}{2.4g}=\frac{2}{x}$
x=0.2g
答:生成H2的质量为0.2g.
点评 本题主要考查有关化学方程式的计算.本题比较简单,由反应物的质量可以根据化学方程式直接计算相关物质的质量.

练习册系列答案
相关题目
14.在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识正确的是C
A.该反应属于分解反应 B.反应中N、Q的质量比为5:3
C.物质P可能是该反应的催化剂 D.X=13.
| M | N | P | Q | |
| 反应前质量(g | 18 | 1 | 2 | 32 |
| 反应后质量(g | X | 26 | 2 | 12 |
C.物质P可能是该反应的催化剂 D.X=13.
11.下列实验操作中,错误的是( )
| A. |  滴加液体 | B. |  加热液体 | C. |  稀释浓硫酸 | D. |  检查气密性 |
8.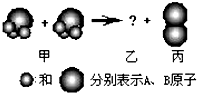 如图所示,两个甲分子反应生成X个乙分子和Y个丙分子,则从图示获得的信息中,正确的是( )
如图所示,两个甲分子反应生成X个乙分子和Y个丙分子,则从图示获得的信息中,正确的是( )
 如图所示,两个甲分子反应生成X个乙分子和Y个丙分子,则从图示获得的信息中,正确的是( )
如图所示,两个甲分子反应生成X个乙分子和Y个丙分子,则从图示获得的信息中,正确的是( )| A. | 分子的种类在化学反应中未发生了改变 | |
| B. | 反应生成的物质丙属于单质 | |
| C. | 该反应的反应类型为化合反应 | |
| D. | X与Y之比等于1:3 |
12.工业酒精中含有甲醇,其结构如图所示,关于甲醇的下列叙述正确的是( )


| A. | 甲醇分子由1个氢原子、4个碳原子和一个氧原子构成 | |
| B. | 甲醇分子中碳、氢元素的质量比为3:1 | |
| C. | 甲醇中所含的质子数和电子数一定相等 | |
| D. | 甲醇由碳、氢、氧三个元素组成 |
13.把50g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需加水( )
| A. | 245g | B. | 195 g | C. | 49 g | D. | 196 g |
 ,用化学符号表示下列微粒:
,用化学符号表示下列微粒: