题目内容
20.为了预防碘缺乏病,国家规定每千克食盐应含有40~60毫克的碘酸钾(KIO3),检验某种食盐是否为加碘的合格食盐,一般过程是取一定量的食盐样品,将其溶解并酸化,加入足量的碘化钾,使碘化钾全部转化为碘单质(I2),再用一定量的硫代硫酸钠(Na2S2O3)溶液与生成的I2恰好完全反应,发生的化学反应过程可表示为:KIO3+5KI+3H2SO4+6Na2S2O3=3H2O+3K2SO4+6NaI+3Na2S4O6
根据消耗的Na2S2O3可以计算得知加碘食盐是否为合格产品.
在一次检验中,取了428g食盐样品,消耗了溶质质量分数为0.5%的Na2S2O3溶液 18.96g,请你计算说明该加碘食盐样品是否为合格产品.(注:1g=1000mg)
分析 根据化学方程式计算碘酸钠的质量,然后与题中的标准进行比较计算,分析是否合格.
解答 解:设食盐中含有碘酸钾的质量为x
KIO3+5KI+3H2SO4+6Na2S2O3=3H2O+3K2SO4+6NaI+3Na2S4O6,
214 948
x 18.96g×0.5%
$\frac{214}{x}$=$\frac{948}{19.96g×0.5%}$
x=0.0214g=21.4mg,
所以1000g食盐中含KIO350mg,因此是合格产品.
故答案为:428g食盐中含KIO321.4mg,1000g食盐中含KIO350mg,因此是合格产品.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列物质中,不能跟NaOH 溶液发生反应的是( )
| A. | CuO | B. | SO2 | C. | H2SO4 | D. | CuCl2 |
8.下列物质不属于溶液的是( )
| A. | 生理盐水 | B. | 医用消毒酒精 | C. | 碘酒 | D. | 蒸馏水 |
5.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 除去稀硝酸中的稀硫酸 | 加入适量硝酸钡溶液,过滤 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在足量的稀硫酸中 |
| D | 除去二氧化碳中的一氧化碳 | 将燃着的木条伸入其中 |
| A. | A | B. | B | C. | C | D. | D |
4.“珍爱生命,远离毒品”.冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N).有关甲基苯丙胺的说法正确的是( )
| A. | 属于混合物 | B. | 一个分子中原子总数为25 | ||
| C. | 燃烧只生成二氧化碳和水 | D. | 氢元素和氮元素的质量比为15:14 |
1.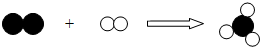 以下是某化学反应的微观示意图(
以下是某化学反应的微观示意图(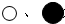 分别表示不同元素的原子),下列对图示反应的理解中,正确的是( )
分别表示不同元素的原子),下列对图示反应的理解中,正确的是( )
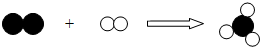 以下是某化学反应的微观示意图(
以下是某化学反应的微观示意图( 分别表示不同元素的原子),下列对图示反应的理解中,正确的是( )
分别表示不同元素的原子),下列对图示反应的理解中,正确的是( )| A. | 反应物和生成物中共含有三种元素 | |
| B. | 参加反应的物质分子个数之比为1:1 | |
| C. | 该反应属于化合反应 | |
| D. | 反应物和生成物中只有一种单质 |