题目内容
18.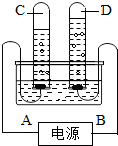 如图是电解水的简易装置:
如图是电解水的简易装置:(1)由图中可知,A为电源的负极,C试管中收集到的气体是氢气,C.D中两气体的质量比为1:8
(2)根据上述事实可经得出结论:水是由氢、氧元素组成的;水是由水分子构成的,在该化学反应中的最小粒子是氢原子和氧原子,生成的新的粒子是氢分子和氧分子.
分析 可以根据电解水方面的知识进行分析、判断,从而得出正确的结论.
解答 解:(1)与正极相连的试管生成的气体是氧气,较少,能支持燃烧.与负极相连的试管生成的是氢气,较多,能燃烧.氢气的体积是氧气体积的2倍.氧气的质量为氢气质量的8倍,故填:负;氢气;1:8.
(2)根据以上实验事实得出:水是由氢元素和氧元素组成的.水是由水分子构成的,电解过程中,水分子分成氢原子和氧原子,然后每两个氢原子重新组合成一个氢分子,每两个氧原子重新组合成一个氧分子,故答案:氢、氧元素,水分子,氢原子和氧原子,氢分子和氧分子.
点评 本题主要考查学生对电解水实验的掌握情况.学生只要熟知此实验的过程、现象,能正确书写反应的化学方程式,就能轻松答题.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
10.将一定量的稀HCl加入到盛有NaOH溶液的烧杯中,未观察到明显现象.对“反应后溶液中的溶质是什么?”同学们提出了以下的猜想:
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
根据上述实验结果,同学们得出猜想二是正确.
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 | 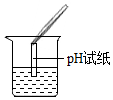 | 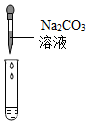 |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
8.下列变化属于化学变化的是( )
| A. | 水果榨汁 | B. | 海水晒盐 | C. | 蜡烛燃烧 | D. | 冰山融化 |
 化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号.
化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号. (1)如图是某趣味实验装置图,挤压胶头滴管后,可观察到气球变大,其是原因用化学方程式表示为:2NaOH+CO2═Na2CO3+H2O.
(1)如图是某趣味实验装置图,挤压胶头滴管后,可观察到气球变大,其是原因用化学方程式表示为:2NaOH+CO2═Na2CO3+H2O.