题目内容
金属加工后的废切削液中含2~5%的NaNO2(一种盐),它是一种环境污染物.人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质.该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2
第二步:NH4NO2
N2↑+2X
请回答以下各题.
(1)第一步反应属于化学反应基本类型中的 .
(2)第二步反应中X的化学式是 .
(3)在NH4NO2中,N的质量分数是 .
第一步:NaNO2+NH4Cl=NaCl+NH4NO2
第二步:NH4NO2
| ||
请回答以下各题.
(1)第一步反应属于化学反应基本类型中的
(2)第二步反应中X的化学式是
(3)在NH4NO2中,N的质量分数是
考点:物质的相互转化和制备,元素的质量分数计算,反应类型的判定,质量守恒定律及其应用
专题:物质的制备
分析:(1)根据反应的特点分析反应的类型;
(2)根据质量守恒定律原子的种类、数目不变分析X的化学式;
(3)根据化学式的意义计算NH4NO2中,N的质量分数.
(2)根据质量守恒定律原子的种类、数目不变分析X的化学式;
(3)根据化学式的意义计算NH4NO2中,N的质量分数.
解答:解:(1)在NaNO2+NH4Cl=NaCl+NH4NO2中,是两种化合物相互交换成分生成了两种新的化合物,属于复分解反应;
(2)在NH4NO2
N2↑+2X的左边有氮、氢、氧原子的个数分别是:2、4、2,在右边有氮原子的个数是2,由质量守恒定律原子的种类、数目不变可知,X的化学式是H2O;
(3)在NH4NO2中,N的质量分数是:
×100%=43.75%.
故答为:(1)复分解反应;(2)H2O;(3)43.75%.
(2)在NH4NO2
| ||
(3)在NH4NO2中,N的质量分数是:
| 14×2 |
| 14×2+1×4+16×2 |
故答为:(1)复分解反应;(2)H2O;(3)43.75%.
点评:解答本题关键要掌握常见反应类型的判断方法、质量守恒定律和有关化学式的计算的判断等知识.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
下列物质由离子构成的是( )
| A、铜 | B、氯化钠 |
| C、二氧化碳 | D、金刚石 |
下列对实验现象的观察和分析合理的是( )
| A、向某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有CO32- |
| B、向某溶液中滴入BaCl2溶液,生成不溶于HNO3的白色沉淀,该溶液中一定含有SO42- |
| C、向某无色溶液中滴入酚酞试液后显红色,该溶液不一定是碱溶液 |
| D、验证烧碱溶液中是否含Cl-,先加稀盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl- |
 某同学要在实验室中制二氧化碳气体并检验二氧化碳气体,请结合图回答下列问题:
某同学要在实验室中制二氧化碳气体并检验二氧化碳气体,请结合图回答下列问题: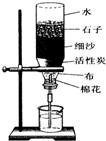 学校、家庭、办公室常用的净水器的基本原理可用如图所示的简易净水装置表示.
学校、家庭、办公室常用的净水器的基本原理可用如图所示的简易净水装置表示.