题目内容
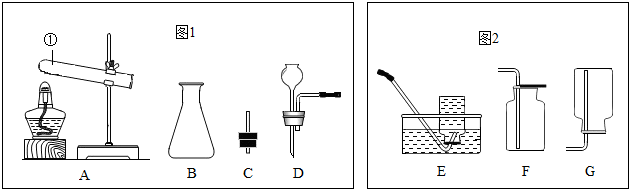
1.请结合如图实验常用装置,回答有关问题.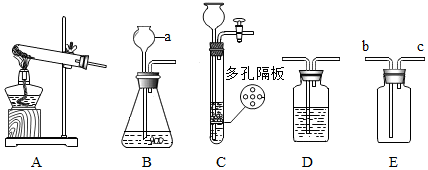
(1)写出图中a仪器的名称:长颈漏斗.
(2)若用高锰酸钾制取氧气,应选用的发生装置是A(填装置序号),在加入药品前,应首先检查装置气密性,在正确选择的发生装置中还存在第一个缺陷,改进的方法是在试管口放一团棉花,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入稀盐酸,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
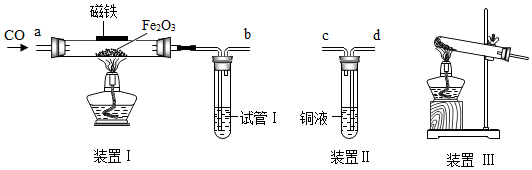
(4)甲烷是一种密度比空气小,难溶于水的气体,实验室常用无水醋酸钠固体和碱石灰固体共热制取甲烷,应选择的发生装置是A(填装置序号),若选用E装置用于排空气法收集 甲烷,甲烷应从c(填“b”或“C”)端通入,若选用D装置用于排水法收集甲烷,瓶中先装满水,甲烷应从右(填“左”或“右”)端通入.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,在加入药品前,应首先检查装置的气密性,实验室用高锰酸钾制取氧气时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据要制取二氧化碳,在B装置中装有石灰石,长颈漏斗中应加入稀盐酸,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(4)根据实验室制取甲烷的反应物是固体,反应条件是加热,甲烷密度比空气小,甲烷难溶于水,密度比水小进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用的发生装置是A,在加入药品前,应首先检查装置的气密性,实验室用高锰酸钾制取氧气时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)要制取二氧化碳,在B装置中装有石灰石,长颈漏斗中应加入稀盐酸,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)实验室制取甲烷的反应物是固体,反应条件是加热,所以应选择的发生装置是A,甲烷密度比空气小,所以选用E装置用于排空气法收集甲烷,甲烷应从c端通入,甲烷难溶于水,密度比水小,所以选用D装置用于排水法收集甲烷,瓶中先装满水,甲烷应从右端通入.
故答案为:(1)长颈漏斗;
(2)A,装置的气密性,在试管口放一团棉花,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)稀盐酸,CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)A,c,右.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 用沉淀法除氢氧化钠中的硝酸钾 | |
| B. | 用结晶法除硝酸钾中少量的氯化钠 | |
| C. | 用碳酸氢钠溶液除二氧化碳中的氯化氢气体 | |
| D. | 用过滤法除粗盐中不溶性杂质 |
| A. | R的化学式一定是CH2O 中 | |
| B. | 6g R完全燃烧消耗氧气6.4g | |
| C. | R中碳元素的质量分数约为85.7% | |
| D. | R仅由C、H两种元素组成,其质量比为6:1 |
①核电荷数相同②核外电子数相等③所含的质子数相等④质量几乎相等.
| A. | ①③④ | B. | ②③④ | C. | ①②④ | D. | ①② |