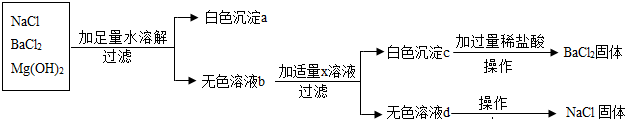
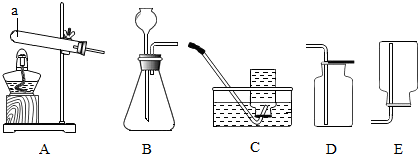
题目内容
15.下列各组溶液,不加其他试剂就不能鉴别的是( )| A. | BaCl2、Na2SO4、K2CO3、HNO3 | B. | NaOH、NaCl、石蕊、稀HCl | ||
| C. | AgNO3、NaCl、CaCl2、HNO3 | D. | CuSO4、NaCl、KOH、HCl |
分析 做这种类型的题首先看有没有带颜色的溶液,再相互结合看是否有沉淀生成,是否有气体放出,在有沉淀生成时要看颜色是否相同.
解答 解:A、将溶液两两混合,有气泡产生的是碳酸钾和硝酸,另外两种是氯化钡和硫酸钠,将能产生气体的两种溶液取其中的一种,与另外两种溶液混合,若是其中一个出现沉淀、一个没有变化,则取的溶液是碳酸钾,能与之产生沉淀的是氯化钡,不产生沉淀的是硫酸钠,剩余的未取的溶液是硝酸,可以鉴别;
B、观察颜色,紫色的是石蕊试液,将石蕊试液与其他的三种溶液混合,石蕊颜色变蓝的,说明是氢氧化钠溶液,石蕊溶液变红的,说明是盐酸,石蕊试液颜色不变的,说明是氯化钠溶液,可以鉴别;
C、将溶液两种混合,硝酸银能与氯化钠和氯化钙反应产生沉淀,故能与其他两种物质产生沉淀的是硝酸银,不与硝酸银反应的是硝酸,但是氯化钠和氯化钙无法鉴别;
D、观察颜色,蓝色的是硫酸铜,将硫酸铜溶液与其他三种溶液分别混合,产生蓝色沉淀的是氢氧化钾溶液,剩余的两种是盐酸和氯化钠溶液,向产生的沉淀中加入剩下的溶液,若是沉淀溶解,则加入的是盐酸,剩余的是氯化钠溶液,可以鉴别;
故选C.
点评 解这类题目的总体思路是:先看颜色,再相互结合,有沉淀、有气体生成的一定能鉴别开.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.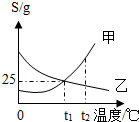 如图为甲、乙两种固体的溶解度曲线,下列说法正确的是( )
如图为甲、乙两种固体的溶解度曲线,下列说法正确的是( )
 如图为甲、乙两种固体的溶解度曲线,下列说法正确的是( )
如图为甲、乙两种固体的溶解度曲线,下列说法正确的是( )| A. | 甲、乙溶解度均随温度升高而增大 | |
| B. | 降温或蒸发均可使乙物质从其饱和溶液中结晶析出 | |
| C. | 甲、乙饱和溶液从t1升温之t2时,其浓度均保持不变 | |
| D. | t1时,甲、乙饱和溶液中溶质和溶剂的质量比均为1:4 |
6.下列图示中的实验操作正确的是( )
| A. | 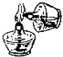 | B. | 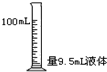 | C. | 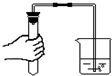 | D. |  |
7.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用熟石灰制生石灰 CaO+H20═Ca(OH)2 化合反应 | |
| B. | 实验室制取氢气 Zn+H2SO4=ZnSO4+H2↑ 置换反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O 氧化反应 | |
| D. | 用碳酸钾制氢氧化钾 2NaOH+K2CO3═Na2CO3+2KOH 复分解反应 |