题目内容
3.小张同学在实验室发现一瓶敞口放置的NaOH固体,他对这瓶NaOH固体的变质情况进行了如下实验探究.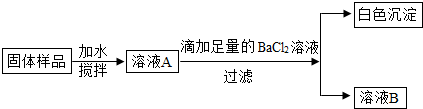
(1)取少量固体于试管中,滴加稀盐酸,有气泡产生现象,由此可知该NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)该同学为进一步探究固体中是否还含有NaOH,设计了如下实验方案:
①滴加足量的BaCl2溶液目的是除尽Na2CO3,生成沉淀的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
②取少量溶液B于试管中,滴加少量酚酞试液,现象为变红,其结论是固体样品中存在(填“存在”或“不存在”)氢氧化钠.
分析 本题是对敞口放置的NaOH固体变质情况的实验探究,变质的原因主要是碱与二氧化碳发生了化学反应.
(1)对于固体加酸有气体产生,说明已变质.
(2)探究固体中是否还含有NaOH,因为碳酸钠溶液也显碱性,故要先排除碳酸钠的干扰;然后根据溶液中加酚酞的颜色变化来判断氢氧化钠的存在.
解答 解:(1)在空气中变质是和二氧化碳发生了化学反应,故答案为:2NaOH+CO2=Na2CO3+H2O;碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,所以加盐酸有气泡冒出;
(2)①足量的BaCl2溶液可将碳酸钠全部反应掉,或除尽溶液中的碳酸钠(或(CO32-);化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl;
②因酚酞遇碱变红色,若还有氢氧化钠,加酚酞溶液变红,反之,不变红,
故答案为:(1)气泡产生; CO2+2NaOH=Na2CO3+H2O
(2)①除尽Na2CO3;BaCl2+Na2CO3=BaCO3↓+2NaCl
②酚酞;变红(或不变色);存在(或不存在)【或其他合理解答】
点评 通过本题学生要明确分析成分,主要是分析可能发生的化学反应,应熟悉物质之间的相互反应及现象.

练习册系列答案
相关题目
13.下列物质敞口放置在空气中较长时间后,质量会增加且没有生成新物质的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 烧碱 | D. | 生石灰 |
18.下列说法正确的是( )
| A. | 煤气泄漏,用明火查看 | B. | 明矾净水,能杀菌消毒 | ||
| C. | 油锅着火,可加水浇灭 | D. | 金属回收,可节能防污 |
 某澄清溶液的溶质由HCl、H2SO4、MgCl2、CuCl2、NaNO3五种中的一种或几种混合而成.
某澄清溶液的溶质由HCl、H2SO4、MgCl2、CuCl2、NaNO3五种中的一种或几种混合而成.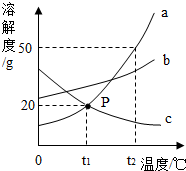 如图是 a、b、c三种物质(均不含结晶水)的溶解度曲线,请回答:
如图是 a、b、c三种物质(均不含结晶水)的溶解度曲线,请回答: