题目内容
9.某同学利用如图所示装置探究燃烧的条件(热水温度远高于白磷着火点).下列说法不正确的是( )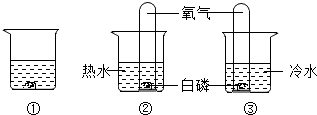
| A. | ①中水为热水 | B. | ②中白磷燃烧 | ||
| C. | ①和③对比可以得出燃烧的条件之一 | D. | ②和③对比可以得出燃烧的条件之一 |
分析 燃烧的条件,也就是:(1)可燃物,(2)氧气(或空气),(3)温度达到着火点.
解答 解:A、①是热水和白磷,由于没有氧气,缺少了可燃物燃烧需要的氧气,不能燃烧,用来和②对比得出飞、燃烧条件的;
B、②中白磷在热水中,试管内有氧气,既有氧气的参与,也达到了着火点,会燃烧;
C、①中水为热水,但无氧气,不能燃烧,③中白磷有氧气,但冷水温度低,达不到着火点,不能燃烧,①和③对比不能得出燃烧的条件;
D、②中白磷在热水中,试管内有氧气,既有氧气的参与,也达到了着火点,会燃烧;,③中白磷有氧气,但冷水温度低,达不到着火点,不能燃烧,故②和③对比可以得出燃烧的条件之一:温度达到着火点.
故选:C.
点评 在解该题时,首先要知道可燃物燃烧的条件,然后比较各个选项,看是否满足可燃物燃烧的三个条件,即可得到答案.

练习册系列答案
相关题目
20.下列物质在空气中燃烧,不能发出蓝色(或淡蓝色)火焰的是( )
| A. | S | B. | H2 | C. | CO | D. | P |
4.如图中“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
| A. | 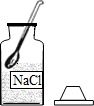 取用氯化钠固体 | B. |  称量氯化钠固体 | C. | 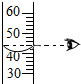 量取水的体积 | D. | 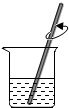 溶解 |
12.某化学兴趣小组根据如图所示进行模拟炼铁的实验,并对产物成分进行探究. 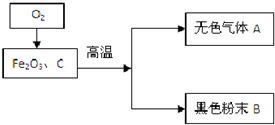
经初步分析:
无色气体 A 不含有单质气体,黑色粉末 B 含有两种单质中的一种或者两种.
高炉炼铁的原理为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$Fe+3CO2 请写出反应器中一氧化碳是如何产生的化学方程式C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
兴趣小组又分成甲乙两组分别对无色气体A 和黑色粉末 B的成分进行探究.
【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的一氧化碳.
乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁. 假设二:只含有碳. 假设三:以上两种物质都含有不用填.
【实验与探究】
(1)为验证甲组的猜想,大家按如图示进行实验(箭头表示气体流向):
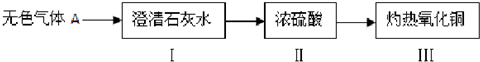
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A 的成分 为:二氧化碳和一氧化碳,Ⅱ中浓硫酸的作用是:干燥气体.
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑.
【交流与反思】
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来:没有进行尾气处理.

经初步分析:
无色气体 A 不含有单质气体,黑色粉末 B 含有两种单质中的一种或者两种.
高炉炼铁的原理为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$Fe+3CO2 请写出反应器中一氧化碳是如何产生的化学方程式C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
兴趣小组又分成甲乙两组分别对无色气体A 和黑色粉末 B的成分进行探究.
【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的一氧化碳.
乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁. 假设二:只含有碳. 假设三:以上两种物质都含有不用填.
【实验与探究】
(1)为验证甲组的猜想,大家按如图示进行实验(箭头表示气体流向):

当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A 的成分 为:二氧化碳和一氧化碳,Ⅱ中浓硫酸的作用是:干燥气体.
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
| 实验方法 | 实验操作 | 实验现象 | 实验结果 |
| 物理方法 | 假设三成立 | ||
| 化学方法 | 取少量黑色粉末B于试管中,加入过量的稀盐酸 | 假设三成立 |
【交流与反思】
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来:没有进行尾气处理.
13.已知浓硫酸比稀硫酸的密度大,质量分数分别为85%和5%的两种硫酸溶液等体积混合后所得溶液的质量分数为( )
| A. | 小于45% | B. | 等于45% | C. | 大于45% | D. | 无法确定 |
 资源、能源、环境与人类的生活和社会发展密切相关.
资源、能源、环境与人类的生活和社会发展密切相关.