题目内容
15. 有一瓶未知浓度的氢氧化钠溶液,同学们想用10%的稀盐酸来测定其溶质的质量分数.以下是两组同学的设想及做法:
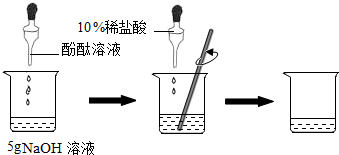
有一瓶未知浓度的氢氧化钠溶液,同学们想用10%的稀盐酸来测定其溶质的质量分数.以下是两组同学的设想及做法:①甲组同学的实验如图所示:在烧杯中加入5g氢氧化钠溶液,滴入2滴酚酞溶液,用滴管慢慢滴入10%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止.请回答:
酚酞溶液的作用是判断反应是否恰好完全反应;
边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是使反应物充分反应.
当溶液颜色恰好变为无色时,共用去了稀盐酸14.6g,则甲组这瓶氢氧化钠溶液中溶质的质量分数为32%(写出计算过程,结果用百分数表示).
②乙组同学的设想是:在烧杯中加入一定量的氢氧化钠溶液,用滴管慢慢滴入10%的稀盐酸,并不断搅拌,通过用pH试纸多次测定溶液pH的办法,达到实验目的.
下列使用pH试纸的方法正确的是AC(填字母).
A.将pH试纸剪成几段节约使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸润湿后放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上
| 实验步骤 | 现 象 | 结 论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液. | 产生白色沉淀,酚酞变红 | NaOH溶液部分变质 |
若要除去溶液中变质生成的杂质,请简要写出实验方案向溶液中滴加氢氧化钡溶液,直至刚好不产生白色沉淀为止,过滤.
分析 ①氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钠和水;
玻璃棒的用途有搅拌、引流、转移物质等;
根据稀盐酸的质量、溶质质量分数可以计算氢氧化钠的质量,进一步可以计算氢氧化钠溶液中溶质的质量分数;
②利用pH试纸测定溶液pH的正确方法是:将pH试纸放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上,再与标准比色卡对照;
氯化钙不能和氢氧化钠反应,能和碳酸钠反应生成碳酸钙沉淀和氯化钠;
稀盐酸能和碳酸钠反应生成氯化钠、水和二氧化碳,能和氢氧化钠反应生成氯化钠和水;
氢氧化钡不能和氢氧化钠反应,能和碳酸钠反应生成白色沉淀碳酸钡和氢氧化钠.
解答 解:①溶液颜色恰好变为无色时,说明氢氧化钠和稀盐酸恰好完全反应,因此酚酞溶液的作用是判断反应是否恰好完全反应;
边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是使反应物接触更充分,反应进行更彻底;
设反应的氢氧化钠的质量为x,
NaOH+HCl═NaCl+H2O,
40 36.5
x 14.6g×10%
$\frac{40}{x}$=$\frac{36.5}{14.6g×10%}$,
x=1.6g,
则甲组这瓶氢氧化钠溶液中溶质的质量分数为:$\frac{1.6g}{5g}$×100%=32%.
故填:判断反应是否恰好完全反应;使反应物充分反应;32%.
②A.将pH试纸剪成几段使用,既不影响实验结果,又节约pH试纸,该选项说法正确;
B.将pH试纸直接插入待测液中时,会污染待测液,该选项说法不正确;
C.将pH试纸放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上,再与标准比色卡对照即可知待测液的pH,该选项说法正确;
D.将pH试纸润湿后放在干净的表面皿上,用玻璃棒蘸取待测液滴在pH试纸上时,能使待测液的质量分数减小,碱性减弱,从而导致测定的pH偏小,该选项说法不正确;
实验步骤、实验现象和结论如下表所示:
| 实验步骤 | 现 象 | 结 论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液 | 产生白色沉淀,酚酞变红 | NaOH溶液部分变质 |
若要除去溶液中变质生成的杂质碳酸钠,实验方案是:向溶液中滴加氢氧化钡溶液,直至刚好不产生白色沉淀为止,过滤,即可除去碳酸钠.
故填:AC;产生白色沉淀,酚酞变红;向溶液中滴加氢氧化钡溶液,直至刚好不产生白色沉淀为止,过滤.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 酚酞试液 | B. | 稀盐酸 | C. | 碳酸钠溶液 | D. | 硫酸铜溶液 |
| A. | 医疗上用作“钡餐”的硫酸钡 | B. | 作为绿色能源的酒精 | ||
| C. | 一种国际上限制排放的温室气体 | D. | 一种常见的含氧酸 |
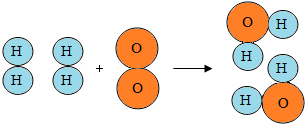
| A. | 氧气由氧原子构成 | |
| B. | 反应中氢原子和氧原子都发生了变化 | |
| C. | 反应前后元素的化合价发生了变化 | |
| D. | 水是氢元素和氧元素组成的混合物 |
| A. | 回收利用废旧金属,变废为宝 | |
| B. | 改变燃料的组成和结构,减少工业烟尘和各种有害气体的排放,保护大气资源 | |
| C. | 减少“白色污染”,集中收集并焚烧废弃塑料 | |
| D. | 加强生活污水处理,保护水资源 |

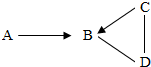 固体A、气体B以及溶液C、D之间有如图所示转化关系,“-”表示两种物质之间可以相互反应,但不能直接转化.天然存在的A是重要的建筑材料.则A、B的化学式分别是CaCO3、CO2.B与D反应的一种产物可以用于实现C到B的转化,该物质可能是Na2CO3.
固体A、气体B以及溶液C、D之间有如图所示转化关系,“-”表示两种物质之间可以相互反应,但不能直接转化.天然存在的A是重要的建筑材料.则A、B的化学式分别是CaCO3、CO2.B与D反应的一种产物可以用于实现C到B的转化,该物质可能是Na2CO3.