题目内容
8.取氢氧化铜和氢氧化镁组成的混合物7.8g,放入一定质量的溶质质量分数为10%的稀硫酸中,恰好完全反应,将所得溶液蒸发得到固体14g.则所用稀硫酸溶液的质量是( )| A. | 50g | B. | 100g | C. | 49g | D. | 98g |
分析 根据氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化镁和硫酸反应生成硫酸镁和水,依据质量守恒定律进行计算.
解答 解:氢氧化铜和硫酸反应生成硫酸铜和水,氢氧化镁和硫酸反应生成硫酸镁和水,化学方程式为:Mg(OH)2+H2SO4=MgSO4+2H2O,Cu(OH)2+H2SO4=CuSO4+2H2O依据化学方程式可知,金属元素反应前后质量不变,反应固体增加的质量就是氢氧根离子和硫酸根离子的质量差,依据关系式可知,
设稀硫酸的质量为x
H2SO4----2OH----S${{O}_{4}}^{2-}$---增加的质量
98 34 96 62
x×10% 14g-7.8g
$\frac{98}{x×10%}$=$\frac{62}{14g-7.8g}$
x=98g
故选:D.
点评 本题主要考查了质量守恒定律的应用,难度不大,注意认真分析反应原理即可解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列关于碳及其化台物的说法错误的是( )
| A. | 石墨、金刚石和C60的物理性质不同,但都属于碳的不同物质 | |
| B. | CO具有还原性,能将CuO还原成Cu | |
| C. | 含碳的化合物中甲烷、乙醇属于有机物,CO、CO2则属于无机物 | |
| D. | CO与CO2均有毒 |
3.水中的氮、磷、钾超过一定含量即为水质的富营养化,会导致水藻因养分过足而迅速生长繁殖.一部分大量生长繁殖,另一部分大量死亡,使水质变得混浊不堪,就出现了藻华现象.测定水样中磷的含量时,需要用到钼酸铵,化学式(NH4)2MoO4,已知NH4+原子团的化合价为+1,则Mo的化合价是( )
| A. | +7 | B. | +6 | C. | +4 | D. | +1 |
17.下列说法正确的是( )
| A. | 油脂属于高分子化合物 | |
| B. | 豆油、猪油、汽油都属于油脂 | |
| C. | 加碘食盐遇到淀粉水溶液后会变蓝 | |
| D. | 谷物、甘薯在酿酒过程中,淀粉不能直接转化为乙醇 |

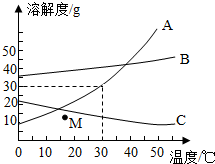 A、B、C三种物质溶解度曲线如图所示,回答下列问题:
A、B、C三种物质溶解度曲线如图所示,回答下列问题: