题目内容
3.将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中充分反应后过滤,将滤渣放入稀盐酸溶液里,有气泡产生.则下列情况不可能存在的是( )| A. | 滤渣是Ag、Cu、Zn | B. | 滤渣是Ag、Cu、Mg | ||
| C. | 滤液中含有Zn2+、Mg2+、NO3- | D. | 金属活动性顺序是Ag<Cu<Zn<Mg |
分析 镁比锌活泼,锌比铜活泼,铜比银活泼,将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中时,锌不能和硝酸镁反应,先和硝酸铜反应,后和硝酸银反应;
锌能和稀盐酸反应生成氯化锌和氢气,而铜和银都不能和稀盐酸反应.
解答 解:A、将滤渣放入稀盐酸溶液里,有气泡产生,说明锌过量,滤渣中含有锌,同时含有锌和硝酸铜、硝酸银反应生成的铜和银,该选项说法正确;
B、镁比锌活泼,因此锌不能和硝酸镁反应,滤渣中不含有镁,该选项说法不正确;
C、滤液中含有反应生成的锌离子和没有反应的镁离子,同时含有硝酸根离子,该选项说法正确;
D、金属活动性顺序是Ag<Cu<Zn<Mg,该选项说法正确.
故选:B.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
13.如图所示进行有关碳及其氧化物的性质实验,不正确的说法是( )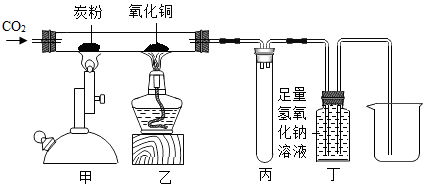

| A. | 甲、乙两处的现象分别是:黑色粉末减少,黑色粉末逐渐变红 | |
| B. | 甲处发生的反应是典型的吸热反应 | |
| C. | 丙处试管可防止液体倒吸 | |
| D. | 该装置的不足之处是未进行尾气处理 |
15.一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
| A. | 鸡蛋清显碱性 | B. | 胃酸过多的人应少吃泡菜 | ||
| C. | 橘子汁能使紫色石蕊溶液变红 | D. | 牛奶比橘子汁的酸性强 |
3.下列四个图象中,能正确反映对应变化关系的是( )
| A. | 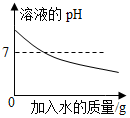 在常温下,稀释KOH溶液,加入水的质量与溶液pH变化的关系 | |
| B. | 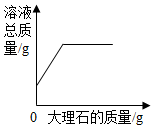 向一定量的稀盐酸中加入大理石,溶液的总质量随加入的大理石的质量关系 | |
| C. | 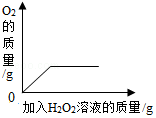 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液,产生的氧气与加入的过氧化氢溶液的情况 | |
| D. | 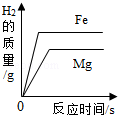 将等质量的镁片和铁片投入到足量稀硫酸中,产生氢气的质量随时间变化关系 |
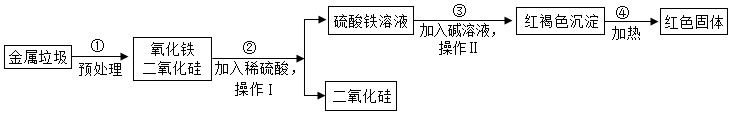
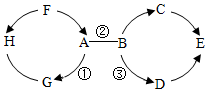 A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).
A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“-”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).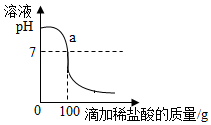 将含有NaCl杂质的某烧碱样品10g完全溶于90g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸.在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示.
将含有NaCl杂质的某烧碱样品10g完全溶于90g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸.在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示.