题目内容
4.根据如图所示的实验回答问题: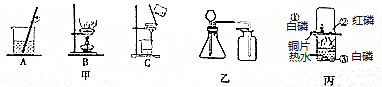
(1)给氯酸钾和二氧化锰的混合物充分加热制得所需的氧气后,为了分离、回收反应后固体中的二氧化锰和氯化钾,应将反应后的混合物依次经过操作(甲图中的):A、C,再将得到的黑色固体用蒸馏水冲洗、晾干可得到二氧化锰,然后将得到的液体进行操作;B可得到氯化钾固体.
图甲中某图操作有一处错误,指出该图操作的具体错误:没有用玻璃棒搅拌;图甲-C中玻璃棒的作用是引流.
(2)实验室可用图乙能制取H2、O2、CO2中哪两种气体?O2、CO2;.怎样通过实验证明此气体是这两种气体中的哪一种气体?用带火星的木条放在集气瓶内,如果复燃,则证明是氧气.如果该气体是光合作用的产物,写出用此图发生装置制取该气体的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)对于图丙:罩上烧杯的作用是防止生成的五氧化二磷污染空气;对照①和③能够得到可燃物燃烧需要的条件之一是氧气.
分析 (1)实验室分离混合物的基本操作有:过滤、蒸发.做题时需要根据不同混合物的特点具体分析.
(2)根据实验室制取H2、O2、CO2的反应原理及气体的收集方法解答;
(3)根据燃烧的条件分析解答.
解答 解:滤渣是氯化钾、二氧化锰的混合物,氯化钾可溶于水,但二氧化锰不溶于水,所以先把混合物溶解,然后过滤,就可以得到氯化钾溶液,再用蒸发结晶的方法,可得到氯化钾晶体.图甲中没有用玻璃棒搅拌,图甲-C中玻璃棒的作用是引流;
(2)实验室制取H2、O2、CO2的反应原理都是固体和液体在常温下反应,属于固液常温型,氢气的密度比空气的小,用向下排空气法收集;氧气、二氧化碳的密度比空气的大,用向上排空气法收集;实验室可用图乙能制取O2、CO2;用带火星的木条放在集气瓶内,如果复燃,则证明是氧气,如果该气体是光合作用的产物,说明是氧气,实验室用二氧化锰和过氧化氢制取氧气,属于固液常温型,故选发生装置B,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)磷燃烧生成五氧化二磷,易污染空气,对于图丙:罩上烧杯的作用是防止生成的五氧化二磷污染空气;对照①和③能够得到可燃物燃烧需要的条件之一是需要氧气.
答案:
(1)A;C;B;没有用玻璃棒搅拌;引流;
(2)O2、CO2;用带火星的木条放在集气瓶内,如果复燃,则证明是氧气;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)防止生成的五氧化二磷污染空气;氧气.
点评 过滤过程中要做到“一贴、二低、三靠”,一贴即滤纸紧贴漏斗边缘,二低即滤纸低于漏斗边缘、滤液低于滤纸边缘,三靠即烧杯紧靠玻璃棒、玻璃棒紧靠三层滤纸、漏斗下端口紧靠烧杯内壁.蒸发操作中要注意当有较多固体出现时就要停止加热,剩下的液体余温可以蒸发干.

| A. | 4.8% | B. | 10.7% | C. | 85.6% | D. | 10.2% |
| A. | 组成元素一定相同 | |
| B. | 构成分子的原子个数一定相同 | |
| C. | 性质、组成和结构完全相同 | |
| D. | 分子中某些原子的结合方式可能是相似的 |
| 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
| A. | 氧化铜 | B. | 氧化铝 | C. | 氧化铁 | D. | 氧化镁 |

 某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.
某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.