题目内容
20.下列表示禁止吸烟的标志是( )| A. |  | B. |  | C. |  | D. |  |
分析 解答本题可根据图中所示标志的含义及题目的要求进行分析判断即可.
解答 解:
A、图中所示标志是禁止烟火标志,故选项错误.
B、图中所示标志是禁止燃放鞭炮标志,故选项错误.
C、图中所示标志是禁止吸烟标志,故选项正确.
D、图中所示标志是当心爆炸---爆炸性物质标志,故选项错误.
故选:C.
点评 本题难度不大,了解各个标志所代表的含义是解答此类题的关键.

练习册系列答案
相关题目
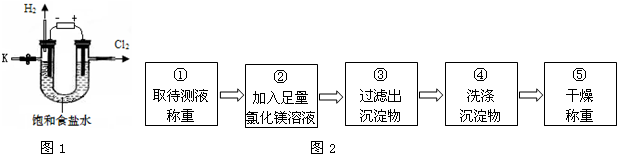
11.某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图1所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.
老师提示:I.电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对以下实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加
入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据
如下:
(2)写出氢氧化钠与稀盐酸反应的化学方程式:NaOH+HCl═NaCl+H2O.
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按图2所示的实验步骤进行实验:
(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是氢氧化镁.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
老师提示:I.电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑

Ⅱ.忽略其他可能发生的反应对以下实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
向待测液中滴加几滴酚酞试液 | 酚酞试液变红色 | 待测液呈碱性,表明含有氢氧化钠 |
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加
入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据
如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按图2所示的实验步骤进行实验:
(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是氢氧化镁.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
15.下列化学式书写错误的是( )
| A. | Na2O | B. | CaCo3 | C. | AlCl3 | D. | Cu(OH)2 |
5.下列实验操作顺序正确的是( )
| A. | 检查装置的气密性,先用手握住试管,再将导管伸入水中 | |
| B. | 制取氧气时,先装入药品,再检查气密性 | |
| C. | 排水法收集氧气时,先将导管伸入充满水的集气瓶中,再加热 | |
| D. | 排水法收集氧气结束后,先将导管从水中取出,再熄灭酒精灯 |
12.有关分离液态空气制氧气的说法正确的是( )
| A. | 利用了液氮比液氧的沸点低 | B. | 制得的氧气为纯氧 | ||
| C. | 发生的是化学变化 | D. | 贮存氧气是在黑色钢瓶中 |
