题目内容
4.根据下列实验装置图填空: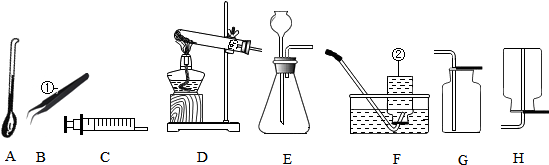
(1)写出图中标示的仪器名称:①镊子,②集气瓶.
(2)实验室用KMnO4制取较纯净的O2,应选用的发生装置为D(填字母序号,下同),收集装置为F,取用KMnO4药品时,应选用仪器把药品小心地送至试管底部,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)组装发生装置D时,下列仪器用品的组装正确顺序是:
铁架台→木块→②→①.(填写以下序号)
①试管②酒精灯
(4)注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至浸没长颈漏斗末端处.
②将注射器C连接到装置E的导管口处,向前推进注射器活塞,若观察到C(选填以下字母)时,则说明E装置气密性良好.
A.长颈漏斗口有气泡冒出
B.锥形瓶中液面上升
C.长颈漏斗中液面上升,并形成稳定水柱
(5)在实验室中,I装置被称做“多功能瓶”,有多种用途,请观察装置的特点回答下列问题:
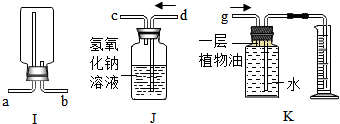
①用排空气法收集气体时若用I装置替代G装置,则气体应从b口进入(填a或b).
②从J、K装置中任选一个,简要阐述该装置的用途:J装置可用于除去气体中混有的CO2或HCl等酸性气体(或K装置用于测定生成气体的体积).
分析 (1)熟记仪器的名称;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)组装仪器时,一般是先下后上,先左后右;
(4)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(5)据气体的密度确定进气口,并结合仪器的作用回答.
解答 解:(1)①是镊子,②是集气瓶;故填:镊子;集气瓶;
(2)实验室用KMnO4制取氧气时需要加热,应该用D装置作为发生装置;因为氧气的密度比空气大,可以用向上排空气法收集,即用G装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;取用KMnO4药品时,应选用仪器药匙把药品小心地送至试管底部;该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.故填:D;F;药匙;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)组装发生装置D时,下列仪器用品的组装正确顺序是:铁架台→木块→酒精灯→试管.故填:②;①.
(4)①向锥形瓶中加入少量水至浸没长颈漏斗末端.
故填:浸没长颈漏斗末端.
②将注射器C连接到装置E的导管口处,向前推进注射器活塞,若看见长颈漏斗中液面上升,并形成稳定水柱时,则说明E装置气密性良好.
故填:C.
(5)①实验室收集氧气若用I装置替代G装置,因为氧气的密度比空气大,而集气瓶倒置,所以应该从短管进气,将空气挤压到集气瓶上部排出;
②J装置可用于除去气体中混有的CO2或HCl等酸性气体,K装置可通过排出水的体积,用于测定生成不溶于水的气体的体积;
故填:①b;②J装置可用于除去气体中混有的CO2或HCl等酸性气体(或 K装置用于测定生成气体的体积)(合理均可).
点评 本题考查知识比较综合,关于气体的制取是中考的常考点,掌握相关知识才能据题意灵活解答,能较好培养学生分析、应用知识解决问题的能力.

 金博士一点全通系列答案
金博士一点全通系列答案| A. | 碳在氧气中燃烧发出白光 | B. | 硫在氧气中燃烧发出淡蓝色的火焰 | ||
| C. | 铁丝在氧气中燃烧生成四氧化三铁 | D. | 磷在空气中燃烧放出白雾 |
| A. | CO2、Fe2O3、H2SO4、O2等都含氧元素,都属于氧化物 | |
| B. | 生铁含碳量2%~4.3%,钢含碳量0.03%~2% | |
| C. | 可燃物与氧气发生的反应都是剧烈的化合反应 | |
| D. | 凡是生成盐和水的反应都是中和反应 |
| A. | K2CO3 | B. | NH4NO3 | C. | P2O5 | D. | Ca3(PO4)2 |
| A. | 氮气可用作保护气,说明氮气不与任何物质发生反应 | |
| B. | 做硫在氧气中燃烧实验时,在集气瓶中留少量水可吸收二氧化硫 | |
| C. | 氧气易溶于水,可以供给水中植物呼吸 | |
| D. | 常用带火星的木条检验空气中的氧气 |
 某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.
某学习小组对课本中“食盐常用于制氧气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主要部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下研究.老师提示:
I.电解饱和食盐水的化学方程式:
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
| 待测液呈碱性,表明含有氢氧化钠. |
【实验】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:
同学们按如图所示的实验步骤进行实验:
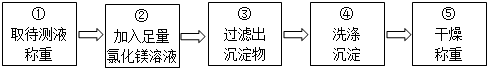
(2)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.步骤④中判断沉淀物是否洗净的具体操作:取最后一次洗涤液少许于试管中,滴加硝酸银溶液,如果不产生白色沉淀,说明已经洗净,如果产生白色沉淀,说明没有洗净(写出实验步骤、现象和结论).
(5)步骤②中发生反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).


 材料的应用,极大地促进了人类社会的发展和人们生活水平的提高.请从化学视角回答下列问题:
材料的应用,极大地促进了人类社会的发展和人们生活水平的提高.请从化学视角回答下列问题: