题目内容
17.通过两个多月的化学学习,我们已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置.请结合如图回答问题: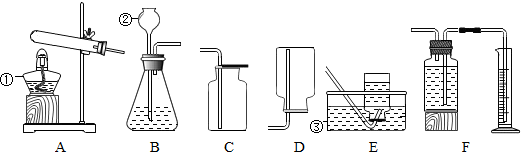
(1)写出图中标有数字的仪器名称:
①酒精灯、②长颈漏斗、③水槽.
(2)实验室用氯酸钾制取氧气,写出反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ 可选用的气体发生装置是A(填编号A、B…,下同);可选用的氧气收集装置是E.实验结束时,应先移出导气管,后熄灭酒精灯,防止水倒流使试管破裂.
(3)如果兴趣小组在实验室改用双氧水和二氧化锰制取氧气,写选用的气体发生装置是B,需要收集30mL的氧气做实验,则最好选择F装置.若需要收集一瓶干燥的氧气,则最好选择C装置.用带火星的木条放在集气瓶口,木条复燃可以证明收集到氧气已满.
(4)现要得到2mol氧气,理论上需要分解多少克过氧化氢?(请写出计算过程)
(5)兴趣小组从网上查到如下信息:用块状大理石与稀盐酸反应可制得二氧化碳气体,且二氧化碳是一种无色无味气体,密度比空气大,能溶于水.于是兴趣小组在实验室选用B气体发生装置制取二氧化碳,又选用C装置收集,并正(填“正”或“倒”)放在桌上准备检验.
分析 (1)根据常见仪器的名称回答;
(2)氯酸钾受热分解生成氯化钾和氧气;发生装置主要由反应物的状态和反应条件决定;选择收集气体的方法时要考虑气体在水中的溶解性和气体与空气密度的相对大小,结合实验的注意事项分析;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
解答 解:(1)①是酒精灯,②是长颈漏斗,③是水槽;故填:酒精灯;长颈漏斗;水槽;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应的方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;氯酸钾是固体且需要加热才能产生氧气,故选择A装置;由于氧气不易溶于水而且密度比空气大,所以收集氧气可用排水法或向上排空气法,再结合题意,需选E才符合;实验结束时,要先把导气管从水槽中取出,然后再熄灭酒精灯,否则水槽里的水会倒流进入试管,热的试管突然遇冷会破裂;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;E;移出导气管;熄灭酒精灯;
(3)过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,过氧化氢是液体,二氧化锰是固体,所以选择B装置,如果用F装置收集氧气,能较准确地测出收集氧气的体积,所以要收集30mL 氧气,就选择F装置;若要收集一瓶干燥的氧气,就不能用排水法,而要用向上排空气法,故选择C;要检验是否收集满了,可用带火星的木条放在集气瓶口,如果复燃说明已经收集满了,否则就没有满;故答案为:B;F;C;带火星的木条放在集气瓶口,木条复燃;
(4)设理论上需要分解xmol过氧化氢
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
2 1
xmol 2mol
$\frac{2}{xmol}$=$\frac{1}{2mol}$ x=4mol m=4mol×34g/mol=136g
答:理论上需要分解136g过氧化氢.
故答案为:136g;
(5)大理石是固体,稀盐酸是液体,而且不用加热,因此实验室制取二氧化碳要选用B装置,由于二氧化碳在水中溶解性较大,通常不用排水法,而是根据它的密度比空气大得多,采用向上排空气法,故选C,检验时集气瓶要正放在桌面上;故答案为:B;C;正.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了实验的注意事项,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 农家肥料的腐烂 | |
| B. | 存放汽油的仓库里接触到火星 | |
| C. | 用蜡烛照明 | |
| D. | 棉花在不通风的地方堆放太多,又长时间不翻动 |
| A. | 质量守恒定律为定量揭示化学变化的规律,提供了理论依据 | |
| B. | 通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量 | |
| C. | 随着科技的发展,精密仪器为我们定量研究化学变化创造了条件 | |
| D. | 质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 |
| A. | Y一定含有氧元素 | B. | 相对分子质量Y>X | ||
| C. | X是碳Y是二氧化碳 | D. | 该反应中X具有还原性 |
| A. | 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 | |
| B. | 酸性溶液的pH小于7.食醋是酸性溶液,所以食醋的pH小于7 | |
| C. | 碱能使无色酚酞变红.氢氧化铜是碱,所以它也能使无色酚酞变红 | |
| D. | 中和反应一定生成盐和水.所以生成盐和水的反应一定是中和反应 |
| A. | 氢气和氧气 | B. | 一氧化碳和氧气 | C. | 天然气和氧气 | D. | 氮气和氧气 |
| A. | 用氢气做燃料 | B. | 用煤做燃料 | C. | 乱扔垃圾 | D. | 露天焚烧秸秆 |
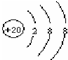 则该元素原子核外有4个电子层,该原子最外层电子数2.该离子是阳离子(填:阴或阳)
则该元素原子核外有4个电子层,该原子最外层电子数2.该离子是阳离子(填:阴或阳)