题目内容
12.精盐(NaCl)和纯碱(Na2CO3)是家庭厨房中两种常见物质.(1)用化学方法区别精盐和纯碱,可以选择下列哪一种物质?答:B.
A.白酒 B.盐酸 C.纯净水 D.酱油
(2)已知:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑,现有精盐(NaCl)和纯碱 (Na2CO3)两种固体混合物53克,加入足量的稀硫酸,充分反应后,生成4.4克二氧化碳气体,则该固体混合物中纯碱(Na2CO3)的质量是多少克?该固体混合物中氯化钠的质量分数是多少?
分析 (1)氯化钠和碳酸钠两种物质都是白色固体,所以不能通过观察颜色来判断.但它们两种物质所含的阴离子不同,所以可以根据阴离子不同来鉴别.
(2)向碳酸钠的氯化钠的固体混合物中加硫酸,氯化钠不与硫酸反应而碳酸钠与硫酸反应生成硫酸钠、水和气体二氧化碳;根据反应中生成二氧化碳的质量,利用反应的化学方程式可计算出混合物中碳酸钠的质量,再计算氯化钠的质量,后求得固体混合物中氯化钠的质量分数.
解答 解:(1)精盐(NaCl)和纯碱(Na2CO3)均溶于纯净水,现象相同,故不能用溶解法来区分.化学反应的现象是多种多样的,所以可以根据化学反应的现象不同来区分.故答案为:各取少许精盐和纯碱于试管中,滴入2毫升稀盐酸,如果有能使澄清石灰水变浑浊的气体产生,证明该物质是纯碱,而另一种物质是精盐.
故选B
(2)设固体混合物中Na2CO3的质量为x,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$,
x═10.6g
该固体混合物中NaCl的质量:20g-10.6g=9.4g
固体混合物中NaCl的质量分数:$\frac{9.4g}{20g}$×100%=47%
答:固体混合物中Na2CO3的质量为10.6g;固体混合物中NaCl的质量分数为47%
点评 氯化钠和纯碱若是在厨房中的,我们可以选择用品尝的方法来区分.但没有指明时,不能用品尝的方法.此题主要考查根据化学方程式的计算,需注意计算步骤的规范、完整性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.空运活鱼必须密封.为了解决鱼的吸氧问题,可在水中加适量的过氧化钙(化学式为CaO2)固体.甲、乙两位同学为弄清“过氧化钙与水反应的产物是什么”,进行了如下探究.
提出问题:把过氧化钙投入足量水中,最终会生成什么物质?
进行猜想:甲同学认为,生成氧化钙和氧气;乙同学认为,生成氢氧化钙和氧气.
(1)你认为哪位同学的猜想是错误的,其理由是甲;氧化钙能与水反应生成氢氧化钙,水溶液中最终产物不可能是氧化钙.
(2)请设计一个实验方案来验证另一位同学的猜想是正确的,并填入下表空格中.
提出问题:把过氧化钙投入足量水中,最终会生成什么物质?
进行猜想:甲同学认为,生成氧化钙和氧气;乙同学认为,生成氢氧化钙和氧气.
(1)你认为哪位同学的猜想是错误的,其理由是甲;氧化钙能与水反应生成氢氧化钙,水溶液中最终产物不可能是氧化钙.
(2)请设计一个实验方案来验证另一位同学的猜想是正确的,并填入下表空格中.
| 实验步骤及操作 | 预期的实验结果 | 结论 |
| ①取少量过氧化钙放入试管中,加足量水,把带火星的木条伸入试管口 | 带火星的木条复燃 | 有氧气生成 |
| ② |
20.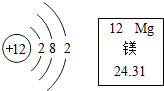 镁有“国防金属”的美誉.镁原子的结构示意图和元素周期表中镁元素的信息如图所示.下列对图中信息解释不正确的是( )
镁有“国防金属”的美誉.镁原子的结构示意图和元素周期表中镁元素的信息如图所示.下列对图中信息解释不正确的是( )
 镁有“国防金属”的美誉.镁原子的结构示意图和元素周期表中镁元素的信息如图所示.下列对图中信息解释不正确的是( )
镁有“国防金属”的美誉.镁原子的结构示意图和元素周期表中镁元素的信息如图所示.下列对图中信息解释不正确的是( )| A. | 镁属于金属元素 | |
| B. | 镁原子的核内质子数为12 | |
| C. | 镁原子的质量为24.31g | |
| D. | 在化学反应中,镁原子容易失去2个电子 |
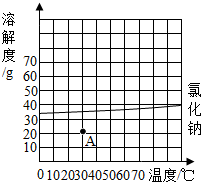 海洋是无价的宝藏,蕴藏着丰富的化学资源.
海洋是无价的宝藏,蕴藏着丰富的化学资源.