题目内容
13. 水是地球上最常见的物质之一,也是人类宝贵的自然资源.
水是地球上最常见的物质之一,也是人类宝贵的自然资源.(1)雪花被人们称为“冬之精灵”,世界上没有两片雪花的形状完全相同.下列说法正确的是D(填选项序号,下同).
A.雪花形成过程中,水分子由运动变为静止
B.雪花融化时,水分子间的间隔没有发生变化
C.不同雪花中,水分子的化学性质不相同
D.不同雪花中,水分子的数目都是巨大的
(2)如图是自来水厂净水过程示意图.

请回答下列问题:
①根据上图信息,生产自来水时使用的净水方法有ABCE.
A.沉淀 B.过滤 C.投药消毒 D.蒸馏 E.吸附
②利用活性炭的吸附性除去水中杂质,该过程属于物理(选填“物理”或“化学”)变化.
③经过上述净水过程,配送给用户的水属于混合物(选填“纯净物”或“混合物”).
④下列关于水的叙述中,正确的是ACD.
A.自然界中的水都是混合物
B.水体有自净能力,不会被污染
C.工业废水经处理达标后才能排放
D.明矾是常用的絮凝剂,可以用来净水
(3)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气.该反应的化学方程式是2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑,此实验可以说明水是由氢元素和氧元素组成的.
(4)氢气和氧气发生反应可以生成水,该反应的过程可用下列图示描述.

上述变化的化学方程式为2H2+O2$\frac{\underline{\;一定条件\;}}{\;}$2H2O;
你从图中还可以看出的信息是原子是化学变化中的最小粒子,此反应是多变一的反应属于化合反应(只填一条即可).
分析 (1)根据分子的定义及特征进行分析,分子是保持物质化学性质的一种粒子,分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;】
(2)根据图示过程回答第一题,根据活性炭具有吸附性,能吸附水中的色素和异味,该过程没有新物质生成,属于物理变化;根据水中含有可溶性杂质,故属于混合物,以及学习的水的有关性质进行解答.
(3)根据题意找出反应物、生成物、反应条件和质量守恒定律进行解答.
(4)由图示可以看出,该反应是氢气与氧气发生反应,燃烧时一般生成对应素的氧化物; 由图示可知,化学变化中的最小粒子是什么,此反应类型等;
解答 解:(1)A、由分子的特征可知,分子是在不断运动的,在雪花的形成过程中,水分子也是不断运动的,故A错误;
B、由分子的特征可知,分子之间有间隔,物质的状态发生变化,就是由于水分子之间的间隔发生变化.故B错误;
C、同种物质的分子性质相同,所以,不同雪花中,水分子化学性质相同.故C错误;
D、由于分子质量和体积都很小,不同雪花中,水分子数目都是巨大的.故D正确;
(2)①根据上图信息,生产自来水时使用的净水方法有沉淀、过滤、投药消毒、吸附,故选ABCE;
②活性炭具有吸附性,能吸附水中的色素和异味,该过程没有新物质生成,属于物理变化;
③经过上述操作后水中还含有可溶性杂质,所以属于混合物;
④A.自然界中的水处在敞开的环境中中,常混入可溶和不可溶性的物质,都是混合物.故A正确;
B.水体虽然有有自净能力,当污染超过自净能力时,就会造成水的污染.故B错误;
C.工业废水经处理达标后才能排放,不会造成水的污染.故C正确;
D.由于明矾溶入水形成的胶状物能够吸附杂质,是常用的絮凝剂,可以用来净水.故D正确.
故选ACD
(3)在TiO2作催化剂和光照条件下,水能分解成氢气和氧气.该反应的化学方程式是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑,氢气中只含有氢元素,氧气中只含有氧元素,故水是由氢元素和氧元素组成的;
(4)由图示可以看出,该反应是氢气与氧气发生反应,化学方程式为:2H2+O2$\frac{\underline{\;一定条件\;}}{\;}$2H2O;
由图示可知,原子是化学变化中的最小粒子,此反应是多变一的反应属于化合反应
故答案为:(1)D;(2)①ABCE;②物理;③混合物;④ACD;(3)2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑;氢元素和氧元素;
(4)2H2+O2$\frac{\underline{\;一定条件\;}}{\;}$2H2O;原子是化学变化中的最小粒子,此反应是多变一的反应属于化合反应;
点评 本题主要考查了有关水的知识,难度不大,这一部分是中考常考的知识点,应加强有关水的知识的学习.

| A. | O2 | B. | N2 | C. | CO | D. | CO2 |
①它们的物理性质不相同 ②它们的化学性质相同 ③它们由不同种分子构成 ④它们为不同的物质 ⑤构成它们的分子相同,但分子之间的间隔不同.
| A. | ①②⑤ | B. | ②③⑤ | C. | ③④⑤ | D. | ①④ |
以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】 化学反应前后各物质的质量总和是否相等?
【查阅资料】 氢氧化钠溶液可以吸收二氧化碳气体
【猜想与假设】 猜想1:不相等;猜想2:相等。
【实验探究】 甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | _________,天平指针没有偏转 |
结论 | 猜想1正确,反应的化学方程 式:_______________. | 猜想2正确 |
【反思评价】 究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_______________中进行。
【优化装置】 同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号)___,从另外两种装置中任选一种指出其不足:________。
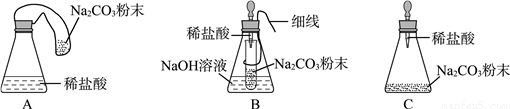
【得出结论】 同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步
分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_________________________的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】
解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_________种元素组成。
 构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法.图中连线两端的物质可以相互反应.下列四组选项中,符合该图要求的是( )
构建知识网络,理清物质间的相互关系,是化学学习中的一种重要方法.图中连线两端的物质可以相互反应.下列四组选项中,符合该图要求的是( )| A. | ①Na2CO3 ②SO2 ③K2CO3 | B. | ①NaHCO3 ②CO2 ③BaCl2 | ||
| C. | ①Fe2O3 ②CO ③Ba(NO3)2 | D. | ①MgO ②SO2 ③Na2CO3 |