题目内容
9.根据如图所示列举的初中常见的装置图,回答下列问题: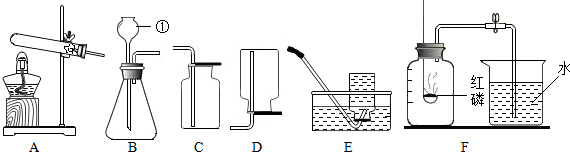
(1)标号为①的仪器的名称是长颈漏斗,盛放红磷的仪器的名称是燃烧匙.
(2)实验室用高锰酸钾制取并收集较纯净氧气的文字表达式是:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,他应选择上述装置中的A和E(填字母)进行组装.
(3)实验室用过氧化氢溶液和二氧化锰制氧气,应该选择的发生装置是B(填字母).
(4)用C装置收集氧气后,验满的方法是把带火星的木条放在集气瓶口,若木条复燃,证明氧气已满.
(5)空气中氧气含量测定的实验装置如图F所示.该实验进行时的主要现象为:红磷燃烧,产生大量白烟,放热,烧杯内的水进入集气,约占集气瓶体积的$\frac{1}{5}$;下列有关此实验的说法正确的是(填字母)C.
A.实验中的红磷越多,水位上升越高
B.燃烧匙中的红磷不可以换成硫和木炭
C.选用足量红磷进行实验是为了耗尽集气瓶内氧气
D.本实验可以证明空气含有N2、O2、CO2和稀有气体.
分析 (1)熟记仪器的名称;
(2)实验室用高锰酸钾制取氧气,属于固体加热型制取气体,据此确定发生装置;根据氧气的密度及溶解性,进行分析解答;
(3)实验室用过氧化氢溶液和二氧化锰制氧气,属于固液常温型,进行分析解答.
(4)根据氧气的验满方法进行分析解答;
(5)根据红磷燃烧产生大量白烟,以及测定空气中氧气含量的实验原理利用红磷燃烧消耗空气中的氧气,使左边集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数去分析解答.
解答 解:(1)①仪器的名称是长颈漏斗;故填:长颈漏斗;盛放红磷的仪器的名称是燃烧匙;
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;属于固体加热型,应该选用的发生装置是A;氧气不易溶于水,用排水法收集的气体比较纯净,则收集装置为E.故填:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;A;E;
(3)实验室用过氧化氢溶液和二氧化锰制氧气,属于固液常温型,应该选择的发生装置是B.故填:B;
(4)用C装置收集氧气后,验满方法为把带火星的木条放在集气瓶口,若木条复燃,证明氧气已满.故填:把带火星的木条放在集气瓶口,若木条复燃,证明氧气已满;
(5)红磷燃烧,产生大量白烟,放热;测定空气中氧气含量的实验原理利用红磷燃烧消耗空气中的氧气,使左边集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数,所以:
A、由于空气中氧气的含量是一定的,当氧气完全反应后,再多的红磷也不和剩余的气体反应,水位就不会再上升,故A错误;
B、由于硫和木炭燃烧时,虽然也消耗空气中氧气但是生成了同是气体的二氧化硫和二氧化碳,导致了集气瓶内体积没有减小,烧杯内的水不会进入集气瓶,故B正确;
C、选用红磷是因为反应可以耗尽氧气,生成固态的P2O5体积减小明显,故C正确;
D、本实验无法证明剩余的气体中含有N2、O2、CO2和稀有气体,只能说明剩余的气体的体积及剩余的气体不和红磷反应、不溶于水,故D错误;
故填:氧气约占空气体积的五分之一;BC.
答案:
(1)长颈漏斗;燃烧匙;
(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;A;E;
(3)B;
(4)把带火星的木条放在集气瓶口,若木条复燃,证明氧气已满;
(5)红磷燃烧,产生大量白烟,放热;烧杯内的水进入集气,约占集气瓶体积的$\frac{1}{5}$;BC.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 阅读快车系列答案
阅读快车系列答案| A. | 面粉是可燃物 | B. | 爆炸一定是化学变化 | ||
| C. | 燃烧爆炸的过程一定有能量的变化 | D. | 面粉厂中应严禁烟火 |
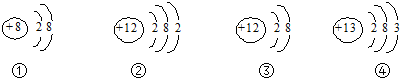
| A. | ①图是一种稀有气体元素的原子结构示意图 | |
| B. | ②图所示的粒子是一种离子 | |
| C. | ②③图所示的粒子化学性质相似 | |
| D. | ③④两图表示的是两种不同元素的微粒 |
| A. | 唾液 6.6-7.1 | B. | 胃液 0.9-1.5 | C. | 汗液 6.6-7.6 | D. | 血浆 7.35-7.45 |
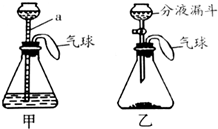 某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:
某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示: