题目内容
15.下列有关说法中,正确的是( )| A. | 原子不显电性,是因为原子中不存在带电的粒子 | |
| B. | 水通电产生氢气和氧气,说明水中含有氢分子和氧分子 | |
| C. | 在化学反应中,反应前后的原子的种类没有改变,数目没有增减 | |
| D. | 不同元素最本质的区别在于相对原子质量不同 |
分析 A、根据原子的构成及微粒的电性分析.
B、根据水的组成考虑;
C、根据化学反应的实质可以解决;
D、根据决定元素种类的微粒考虑.
解答 解:A、原子中的质子带正电,电子带负电,不显电性是因为正负电荷相互抵消的缘故,说法错误.
B、水通电产生氢气和氧气,说明水中含有氢元素和氧元素,水中不存在氢分子和氧分子,故B错;
C、在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化.故C正确.
D、决定元素种类的是核内质子数或核电荷数,所以不同元素最本质的区别是核内质子数不同,故D错.
故选C
点评 解答本题关键是要知道原子不显电性的原因,化学变化的本质是有新物质生成,知道决定元素种类的是核内质子数或核电荷数,知道电解水实验的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.关于水的说法中正确的是( )
| A. | 水由一个氧元素和两个氢元素组成 | B. | 水由氢原子和氧原子构成 | ||
| C. | 水由氢元素和氧元素组成 | D. | 水由一个氧原子和两个氢原子构成 |
10.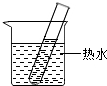 下表是KNO3在不同温度时的溶解度,请回答下列问题
下表是KNO3在不同温度时的溶解度,请回答下列问题
(1)分析表中数据,归纳出KNO3的溶解度随温度变化的规律溶解度随温度的升高而增大.
(2)20℃时,在装有5g KNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为饱和(选填“饱和”或“不饱和”)溶液.该溶液中溶质的质量分数是24.0%(保留一位小数),再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃,此时试管内的溶液中溶质与溶剂的质量比为1:2.
(3)配制一定溶质质量分数的KNO3溶液时,溶解过程所需要的仪器有烧杯、玻璃棒.
 下表是KNO3在不同温度时的溶解度,请回答下列问题
下表是KNO3在不同温度时的溶解度,请回答下列问题| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,在装有5g KNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为饱和(选填“饱和”或“不饱和”)溶液.该溶液中溶质的质量分数是24.0%(保留一位小数),再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃,此时试管内的溶液中溶质与溶剂的质量比为1:2.
(3)配制一定溶质质量分数的KNO3溶液时,溶解过程所需要的仪器有烧杯、玻璃棒.
20.下列关于物质的分类不正确的是( )
| A. | 冰水混合物属于纯净物 | B. | 玻璃属于晶体 | ||
| C. | 像胶、玻璃属于绝缘体 | D. | 不锈钢属于合金 |
7.化学与社会发展及人类的生活关系非常密切,下列有关叙述中正确的是( )
| A. | 经常使用染发剂,对人体健康没影响 | |
| B. | 为保护铝制品,应及时除去表面的氧化膜 | |
| C. | 工业上,常用铁桶来储运烧碱 | |
| D. | 夜晚发现家中燃气泄漏,点火检查泄漏原因 |
4.下列操作正确的是( )
| A. | 实验室用剩的药品应放回原瓶 | |
| B. | 向试管中加块状固体时,先将试管竖直放置,后用镊子将固体放到试管中 | |
| C. | 用手直接拿固体药品 | |
| D. | 称量时,用镊子夹持砝码 |
5.日本福岛发生了核泄漏事故,核电站泄漏出来的放射性物质中含有铯-137,过量摄入铯-137会使人的造血系统和神经系统受到损伤.已知铯-137的质子数为55,中子数为82.下列有关铯-137的说法正确的是( )
| A. | 铯-137原子的核外电子数为82 | B. | 铯-137的相对原子质量为137 g | ||
| C. | 铯-137原子的核电荷数为55 | D. | 铯-137属于非金属元素 |
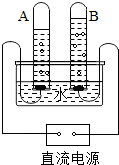 (1)如图是给水通电的简易实验装置.则A试管中产生的气体是氢气,检验B试管内气体的方法是把带火星的木条伸入该气体中,带火星的木条复燃.装置中发生反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(1)如图是给水通电的简易实验装置.则A试管中产生的气体是氢气,检验B试管内气体的方法是把带火星的木条伸入该气体中,带火星的木条复燃.装置中发生反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑