题目内容
化学实验题
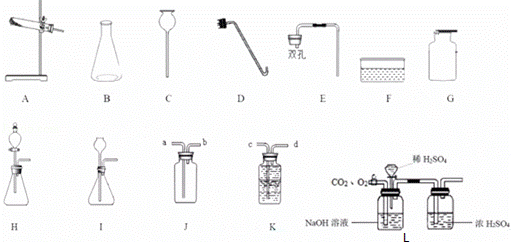
(1)仪器B的名称是 .
(2)写出用KClO3与MnO2的混合固体制取O2的化学方程式 ,需用到的仪器是 (写字母,可多选),那么除此之外还需要用到的仪器是 .
(3)实验室制取CO2的化学方程式是 .
(3)实验室常用块状固体电石(主要成分是CaC2)与水反应制取乙炔,该反应剧烈,速度较快,为了节约化学药品,则应选择的发生装置是 (填字母),通常情况下乙炔(C2H2)是一种无色、无味、密度比空气略小,难溶于水的气体,若要收集较纯净的乙炔气体,则应将气体从 (填a、b、c、或d)通入.
(5)将CO2和O2通入图L进行分离,最终得到的气体是
A.CO2、O2 B.CO2 C.O2 D.O2、H2O.
| 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 常见气体的实验室制法、检验、干燥与净化. |
| 分析: | (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析; (2)根据反应物的状态和反应条件确定实验室制取气体的发生装置,根据氧气的密度和溶水性确定气体的收集装置; (3)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析; (4)根据制取乙炔的反应中所使用药品的状态及反应发生的条件,判断制取该气体时所应选用的发生装置,根据该气体的密度及溶解性,判断收集装置;根据对反应的介绍,确定反应的反应物及生成物,写出反应的化学方程式; (5)根据氢氧化钠会与二氧化碳反应,浓硫酸有吸水性进行分析. |
| 解答: | 解:(1)通过分析题中所指仪器的作用可知,B是锥形瓶; (2)用KClO3与MnO2混合制取和收集纯净O2,反应物的状态是固态,反应条件是加热,所以发生装置选A、D;氧气不易溶于水,所以收集方法选排水法,收集纯净的氧气选F、G;氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3 (3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑; (4)制取乙炔使用固体 (5)氢氧化钠会与二氧化碳反应,浓硫酸有吸水性,所以将CO2和O2通入图L进行分离,最终得到的气体是氧气,故选:C. 故答案为:(1)锥形瓶; (2)2KClO3 (3)CaCO3+2HCl═CaCl2+H2O+CO2↑; (4)H,d; (5)C. |

如图是甲、乙、丙三种固体物质溶解度曲线,下列叙述正确的( )

|
| A. | t2℃时乙物质的饱和溶液溶质的质量分数为20% |
|
| B. | t2℃时三种物质溶解度关系为:甲>乙>丙 |
|
| C. | 随温度的升高,甲、乙、丙三种物质溶解度都增大 |
|
| D. | 甲物质的饱和溶液从t1℃升温到t3℃时,溶质质量分数增大 |
某反应的微观示意图如下,下列说法正确的是( )

|
| A. | 该反应说明原子在化学反应中可再分 |
|
| B. | 反应物的分子个数比为3:2 |
|
| C. | 所有参与反应的物质都是化合物 |
|
| D. | D物质中氮元素的化合价+1 |
下列物质放入水中,不能形成溶液的是( )
|
| A. | 蔗糖 | B. | 植物油 | C. | 食盐 | D. | 食用纯碱 |
下列实验设计能达到实验目的是( )
| 序号 | 实验目的 | 实验方案 |
| A | 检验某气体是否为二氧化碳 | 用燃着的木条 |
| B | 稀释浓硫酸 | 将水缓慢加入浓硫酸中,并搅拌 |
| C | 区分氧化钙与碳酸钙 | 取样品,加入适量水 |
| D | 除去K2S04溶液中的K0H | 加入适量稀盐酸 |
|
| A. | A | B. | B | C. | C | D. | D |
如图所示,实验室里有一套用来制取气体的装置,下列有关叙述正确的是( )
|
| A. | 锥形瓶里加入少量MnO2粉末,分液漏斗里盛放过氧化氢溶液,可以制取氧气 |
|
| B. | 锥形瓶里加入 |
|
| C. | 当发生装置中液体与固体混合产生了气泡,立即开始收集气体 |
|
| D. | 集满氧气的集气瓶从水槽里取出后倒放在实验台上 |
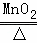 2KCl+3O2↑;因为需要加热,所以还需要酒精灯;
2KCl+3O2↑;因为需要加热,所以还需要酒精灯; 碳化钙与水在常温下发生反应,因此应选用固液不需加热型的发生装置B,由于乙炔(C2H2)是一种难溶于水、密度比空气略小、易燃烧的气体,因此收集时应选用图中装置D的排水法收集;乙炔难溶于水,所以要收集较纯净的乙炔气体,则应将气体从d端通入;
碳化钙与水在常温下发生反应,因此应选用固液不需加热型的发生装置B,由于乙炔(C2H2)是一种难溶于水、密度比空气略小、易燃烧的气体,因此收集时应选用图中装置D的排水法收集;乙炔难溶于水,所以要收集较纯净的乙炔气体,则应将气体从d端通入; 香烟的烟气中含有几百
香烟的烟气中含有几百
 气管的一端插入水中;②缓慢向外拉动注射器的活塞。若观察到 ,则说明装置B不漏气。
气管的一端插入水中;②缓慢向外拉动注射器的活塞。若观察到 ,则说明装置B不漏气。
 大理石,分液漏斗里盛放稀硫酸,可以制取二氧化碳
大理石,分液漏斗里盛放稀硫酸,可以制取二氧化碳