题目内容
10.一个标准碳原子的质量为1.993×10-26 Kg,一个某原子的质量为4.036×10-26 Kg,该原子中原子核内的质子数和中子数相等,通过计算回答:(1)该原子的相对原子质量为多少?
(2)该原子是什么原子?属于哪类元素?(填“金属元素”或“非金属元素”)
分析 根据某原子的相对原子相对质量=$\frac{一个该原子的实际质量kg}{一个碳12原子的实际质量kg×\frac{1}{12}}$进行分析解答本题.
解答 解:(1)根据某原子的相对原子相对质量=$\frac{一个该原子的实际质量kg}{一个碳12原子的实际质量kg×\frac{1}{12}}$则
该原子的相对原子质量=$\frac{4.036×1{0}^{-26}kg}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=24,
(2)根据“该原子中原子核内的质子数和中子数相等”,“该原子的相对原子质量=24”,“相对原子质量=质子数+中子数”,故其质子数是12;则推测该原子为镁原子,属于金属元素;
故答案为:
(1)该原子的相对原子质量为24;(2)镁原子,金属元素.
点评 本题考查的是相对原子质量的理解和应用,一定要注意代入公式时,一定要弄清各个量所代表的含义.

练习册系列答案
相关题目
1.下列化学反应属于氧化反应,但不属于化合反应的是( )
| A. | 碳+氧气→二氧化碳 | B. | 乙醇+氧气→二氧化碳+水 | ||
| C. | 氢气+氧气→水 | D. | 一氧化碳+氧气→二氧化碳 |
18.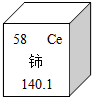 稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
 稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
稀土元素是一类有重要用途的资源.铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )| A. | 铈的原子序数是58 | B. | 铈原子中的质子数为58 | ||
| C. | 铈属于非金属元素 | D. | 铈的相对原子质量是140.1 |
5.下列反应既属于化合反应又属于氧化反应的是( )
| A. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | B. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | ||
| C. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 | D. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
15.我国瓷都--江西景德镇生产的瓷器在世界上享有盛誉.景德镇的高岭土[主要成分Al2(Si2O5)(OH)4]是制造瓷器的优良原料.下列叙述正确的是( )
| A. | 高岭土中氢、氧元素的质量比为4:9 | |
| B. | 高岭土中铝硅元素的质量比是27:28 | |
| C. | 高岭土属于氧化物 | |
| D. | 高岭土由4种元素组成 |
2. 下列关于燃烧与灭火的说法中,正确的是( )
下列关于燃烧与灭火的说法中,正确的是( )
 下列关于燃烧与灭火的说法中,正确的是( )
下列关于燃烧与灭火的说法中,正确的是( )| A. | 将木块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间 | |
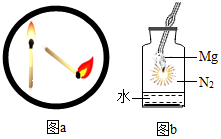
| B. | 如图a,火柴头向下时更容易燃烧,是因为降低了火柴梗的着火点 | |
| C. | 由图b中的现象可知,金属镁引起的火灾不能用氮气灭火 | |
| D. | 蜡烛用扇子一扇即灭,是因为扇走了蜡烛周围的空气 |
 已知A中含有两种元素,B是一种无色的液体、C是气体单质,D是能使燃着的木条熄灭的气体,它们的转化关系如下:
已知A中含有两种元素,B是一种无色的液体、C是气体单质,D是能使燃着的木条熄灭的气体,它们的转化关系如下: