题目内容
某纯碱样品中含有少量氯化钠,现称取纯碱样品15g,溶于50g水配制成溶液,再向其中加入50克CaCl2溶液,恰好完全反应.反应后过滤,称得滤液总重量为105g,
求:(1)根据质量守恒定律,反应生成沉淀的质量为 g;
(2)该纯碱样品中碳酸钠的质量;
(3)反应后所得滤液中溶质的质量分数.
求:(1)根据质量守恒定律,反应生成沉淀的质量为
(2)该纯碱样品中碳酸钠的质量;
(3)反应后所得滤液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据氯化钠、碳酸钠的性质,氯化钠不能与加入的氯化钙发生反应,碳酸钠与氯化钙生成碳酸钙沉淀和氯化钠,溶液减少的质量就是生成的碳酸钙的质量;
(2)根据生成沉淀碳酸钙的质量可计算样品中所含碳酸钠的质量,据此解答即可;
(3)恰好完全反应后所得溶液为氯化钠溶液,此时溶液中的溶质氯化钠由原固体中的氯化钠和反应后生成的氯化钠两部分构成,然后根据滤液的总质量求质量分数.
(2)根据生成沉淀碳酸钙的质量可计算样品中所含碳酸钠的质量,据此解答即可;
(3)恰好完全反应后所得溶液为氯化钠溶液,此时溶液中的溶质氯化钠由原固体中的氯化钠和反应后生成的氯化钠两部分构成,然后根据滤液的总质量求质量分数.
解答:解:(1)根据质量守恒定律,反应生成沉淀的质量为:15g+50g+50g-105g=10g;
故答案为:10g;
设纯碱样品中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g y
=
=
x=10.6g,y=11.7g
(2)答:纯碱样品中碳酸钠的质量为10.6g;
(3)反应后所得滤液中溶质的质量分数:
×100%=15.3%
答:反应后所得滤液中溶质的质量分数为15.3%.
故答案为:10g;
设纯碱样品中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g y
| 106 |
| x |
| 100 |
| 10g |
| 117 |
| y |
x=10.6g,y=11.7g
(2)答:纯碱样品中碳酸钠的质量为10.6g;
(3)反应后所得滤液中溶质的质量分数:
| 15g-10.6g+11.7g |
| 105g |
答:反应后所得滤液中溶质的质量分数为15.3%.
点评:在计算反应后所得溶液的溶质质量分数时,原混合固体中的氯化钠不要忘记算入溶质的质量,此题在这个地方设置一个小陷阱,这也是学生经常出错的地方.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
物质在氧气中燃烧现象正确是( )
| A、铁:火星四射 |
| B、硫:发出淡蓝色火焰 |
| C、木炭:发出红光 |
| D、红磷:产生白雾 |
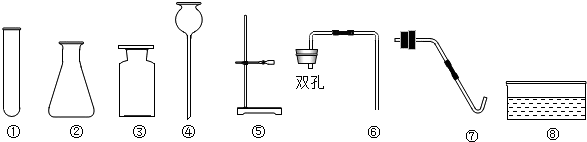
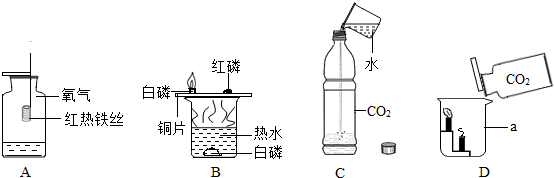
 体味化学魅力,尽享实验神奇.化学老师在元旦化学晚会上表演了神奇的化学实验,请大家一起参与.
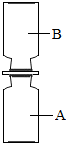
体味化学魅力,尽享实验神奇.化学老师在元旦化学晚会上表演了神奇的化学实验,请大家一起参与.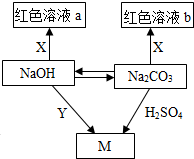 同学们在学习了碱和盐的性质后构建了如图所示的知识网络,其中“→”表示物质之间的转化关系,方框内物质含有相同的金属离子.
同学们在学习了碱和盐的性质后构建了如图所示的知识网络,其中“→”表示物质之间的转化关系,方框内物质含有相同的金属离子.