题目内容
16.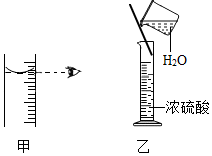 用溶质质量分数为98%(密度1.84g/ml)的浓硫酸配制49g20%的稀硫酸,进行的以下操作和分析正确的是( )
用溶质质量分数为98%(密度1.84g/ml)的浓硫酸配制49g20%的稀硫酸,进行的以下操作和分析正确的是( )| A. | 第一步,计算:需要量取20mL的浓硫酸 | |
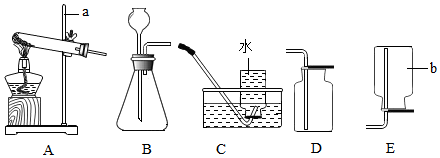
| B. | 第二步,量取:如图甲所示取水 | |
| C. | 第三步,混匀:如图乙操作 | |
| D. | 分析:配成的溶液若向试剂瓶中装瓶时有洒出,会导致瓶中溶液质量质量分数减小 |
分析 A、根据溶液稀释前后溶质的质量不变,进行分析判断.
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
C、根据浓硫酸的稀释方法,进行分析判断.
D、根据溶液具有均一性,进行分析判断.
解答 解:A、设需要量取浓硫酸的体积为x,根据溶液稀释前后溶质的质量不变,则1.84g/ml×x×98%=49g×20% x≈5.43mL,故选项说法错误.
B、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中所示操作正确,故选项说法正确.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中,不能在量筒内稀释浓硫酸,应在烧杯中进行,故选项说法错误.
D、溶液具有均一性,配成的溶液若向试剂瓶中装瓶时有洒出,瓶中溶液质量质量分数不变,故选项说法错误.
故选:B.
点评 本题难度不大,掌握用浓溶液配制稀溶液配制溶质质量分数一定的溶液的基本步骤、溶液稀释前后溶质的质量不变等是正确解答本题的关键.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
11.如表中 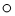 代表氢原子,
代表氢原子,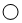 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )
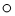 代表氢原子,
代表氢原子,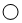 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )| 物质 | ① | ② | ③ | ④ |
| 分子模型 示意图 | 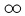 | 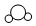 |  | 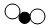 |
| A. | 物质①是单质 | B. | 物质②的相对分子质量为18g | ||
| C. | 物质③中氧元素质量分数最大 | D. | 物质③和④组成的元素相同 |
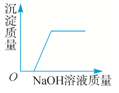
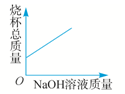
12.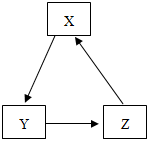 下列表中各组物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
下列表中各组物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
 下列表中各组物质不能按照图中关系(“→”表示反应一步完成)转化的是( )
下列表中各组物质不能按照图中关系(“→”表示反应一步完成)转化的是( ) | 物质 选项 | A | B | C | D |
| X | Na2SO4 | BaCl2 | Cu | CaO |
| Y | NaCl | Ba(NO3)2 | CuO | CaCl2 |
| Z | NaNO3 | BaCO3 | CuSO4 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
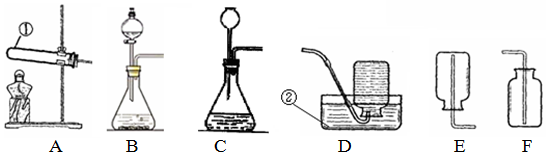
8.对比归纳是学习化学的重要方法.请你参与下列探究活动并回答问题:
实验一:探究影响硫燃烧剧烈程度的因素.
实验二:探究二氧化碳能否与氢氧化钠反应.
实验一:探究影响硫燃烧剧烈程度的因素.
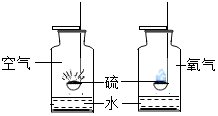 | 如左图,分别将硫在空气和氧气中燃烧. ①硫在氧气里燃烧比在空气里燃烧更剧烈,说明了影响硫燃烧剧烈程度的因素是氧气的浓度. |
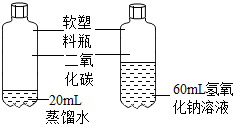 | 左图是小鹏同学设计的对比实验,用于证明二氧化碳和氢氧化钠能否反应.小燕同学认为该实验设计不符合对比实验的基本原则,她的理由是变量不唯一(或水和氢氧化钠溶液的体积不相等). |