题目内容
14.进行化学实验操作考核时,如图四位同学的操作中正确的是( )| A. | 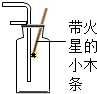 氧气验满 | B. |  给液体加热 | C. |  过滤液体 | D. | 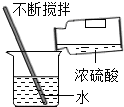 稀释浓硫酸 |
分析 A、根据氧气验满的方法分析判断;
B、根据给试管中的液体加热的方法分析判断;
C、根据过滤液体的方法分析判断;
D、根据浓硫酸的稀释方法分析判断;
解答 解:A、氧气验满时带火星的木条要伸到集气瓶口,故A不正确;
B、给试管里的液体加热时试管里的液体量不能超过试管容积的三分之一,故B不正确;
C、过滤液体时要用玻璃棒引流,故C不正确;
D、稀释浓硫酸时将浓硫酸沿器壁缓缓注入水中,并用玻璃棒不断搅拌,故D正确;
故答案为D.
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
5.小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20.0g此氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如表:
试回答:
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是NaCl、NaOH(写化学式);
(2)计算所测氢氧化钠溶液中溶质的质量分数?
(3)滴加9.9g稀盐酸时,烧杯内溶液中钠元素的质量为0.46g.(计算写过程)
| 加入稀盐酸质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是NaCl、NaOH(写化学式);
(2)计算所测氢氧化钠溶液中溶质的质量分数?
(3)滴加9.9g稀盐酸时,烧杯内溶液中钠元素的质量为0.46g.(计算写过程)
2.下列实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向氢氧化钠固体中加入水 | 氢氧化钠固体消失 | 氢氧化钠与水发生了化学反应 |
| B | 用导管分别对准浸没在热水和冷水中的白磷通氧气 | 热水中的白磷燃烧, 冷水中的白磷不燃烧 | 燃烧条件之一是温度达到着火点 |
| C | 向溶质的质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
| D | 向盐酸和氢氧化钙反应后的溶液中滴加酚酞 | 无明显现象 | 说明盐酸和氢氧化钙恰好反应 |
| A. | A | B. | B | C. | C | D. | D |
6.如图表是元素周期表的一部分,请根据表中提供的信息按要求填空:
(1)由⑤元素组成的单质在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
(2)由①②③三种元素组成的物质的化学式为Na2CO3.
| 3Li 锂 | 4Be 铍 | 5B 硼 | ① | 7N 氮 | ② | 9F 氟 | 10Ne 氖 |
| ③ | 12Mg 镁 | ④ | 14Si 硅 | ⑤ | 16S 硫 | 17Cl 氯 | 18Ar 氩 |
(2)由①②③三种元素组成的物质的化学式为Na2CO3.
4.食用豆腐中含量最多的是亮氨酸(C6H13NO2).下列关于亮氨酸的说法中正确的是( )
| A. | 亮氨酸属于有机高分子化合物 | B. | 亮氨酸中含有氧分子 | ||
| C. | 亮氨酸中氧元素的质量分数最大 | D. | 亮氨酸中氢元素的质量分数为9.9% |
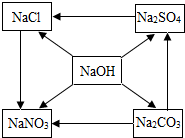 构建知识网络是一种重要的学习方法,如图是某同学整理的关于NaOH性质的知识网络.“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).请回答下列问题:
构建知识网络是一种重要的学习方法,如图是某同学整理的关于NaOH性质的知识网络.“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).请回答下列问题: