题目内容
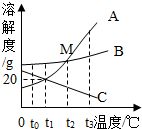 如图所示,根据A、B、C三种物质的溶解度曲线回答问题:
如图所示,根据A、B、C三种物质的溶解度曲线回答问题:(1)t1℃时A物质的溶解度是
(2)M点表示的意义是
(3)A、B、C三种物质的饱和溶液各100g,当问到从t3℃降低到t1℃时,析出晶体(不含结晶水)质量最多的是
(4)要使A物质的不饱和溶液变成饱和溶液可采取的一种方法是
(5)将t3℃时,A、B、C三种物质的饱和溶液降温到t0℃时所形成的溶液中,溶质质量分数由大到小的顺序是
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:根据图示知,A、B两种物质的溶解度随着温度的升高而增大,C物质的溶解度随着温度的升高而降低,且A的溶解度受温度的变化影响比较大,点M是A、B物质在t2℃时溶解度的交点.
解答: 解:(1)如图所示,t1℃时A物质的溶解度是 20g;
解:(1)如图所示,t1℃时A物质的溶解度是 20g;
(2)曲线中交点P表示该温度时两种物质的溶解度相等,所以t2℃时,A、B两种物质的溶解度相等.
(3)C物质的溶解度随着温度的降低而增大,因此降温时不析出晶体;由t3℃时降温到t1℃时,A物质的溶解度差大于B物质的溶解度差,因此t3℃时,等质量的三种物质饱和溶液降温到t1℃时,析出晶体最多的是A物质.
(4)A物质的溶解度随着温度的升高而增大,故将A物质的饱和溶液转变成不饱和溶液可采取加入A物质、蒸发溶剂、降低温度等方法.
(5)饱和溶液的质量分数的计算方法是:
×100%,因为t3℃时A、B、C的溶解度大小是:A>B>C,所以t3℃时A、B、C的饱和溶液的质量分数是A>B>C,降温后A和B都析出晶体,仍然是饱和溶液,又因为t0℃时,B的溶解度大于A的,所以t0℃时,B的饱和溶液的质量分数大于A物质的饱和溶液的质量分数;由于C物质降温后变为不饱和溶质质量分数不变,所以要比较C物质在t3℃时的溶解度与t1℃时A和B物质的溶解度大小,通过图表可知:B>C>A.
故答案为:(1)20;
(2)t2℃时,A、B两种物质的溶解度相等;
(3)A;
(4)降低温度;
(5)B>C>A.
 解:(1)如图所示,t1℃时A物质的溶解度是 20g;
解:(1)如图所示,t1℃时A物质的溶解度是 20g;(2)曲线中交点P表示该温度时两种物质的溶解度相等,所以t2℃时,A、B两种物质的溶解度相等.
(3)C物质的溶解度随着温度的降低而增大,因此降温时不析出晶体;由t3℃时降温到t1℃时,A物质的溶解度差大于B物质的溶解度差,因此t3℃时,等质量的三种物质饱和溶液降温到t1℃时,析出晶体最多的是A物质.
(4)A物质的溶解度随着温度的升高而增大,故将A物质的饱和溶液转变成不饱和溶液可采取加入A物质、蒸发溶剂、降低温度等方法.
(5)饱和溶液的质量分数的计算方法是:
| 溶解度 |
| 溶解度+100g |
故答案为:(1)20;
(2)t2℃时,A、B两种物质的溶解度相等;
(3)A;
(4)降低温度;
(5)B>C>A.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
在化学反应CO2+3H2═□+H2O中,“□”内物质的化学式是( )
| A、CH4 |
| B、CH4O |
| C、CO |
| D、C2H6 |
有X、Y、Z三种金属,如果把X和Y分布放入稀硫酸中,X溶解并产生氢气,而Y不反应,如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化.根据以上实验事实,判断X、Y和Z的金属活动顺序正确的是( )
| A、X>Y>Z |
| B、X>Z>Y |
| C、Z>Y>X |
| D、Z>X>Y |
下列实验现象的描述正确的是( )
| A、硫在氧气中燃烧,发出淡蓝色火焰,产生有刺激性气味的气体 |
| B、镁条在空气中燃烧,发出耀眼的白光,放出热量,生成黑色固体 |
| C、红磷在氧气中燃烧,发出白光,产生大量的白烟 |
| D、蜡烛在氧气中燃烧,发出白光,放出热量,瓶壁上有水雾,澄清的石灰水变浑浊 |