题目内容
18.资料显示:铝与氢氧化钠和水反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.用56.25g含杂质4%的铝片(杂质对产生氢气的质量无影响)与足量的氢氧化钠和水充分反应,生成氢气的质量为多少g.(写出计算过程)分析 依据方程式2A1+2NaOH+2H2O=2NaA1O2+3H2↑,利用铝的质量可以求出生成氢气的质量.
解答 解:设可以制取氢气的质量为X
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
54 6
56.25g×(1-4%) X
$\frac{54}{56.25g×(1-4%)}=\frac{6}{X}$
x=6g
答:生成氢气的质量为6g.
点评 本题主要考查学生对金属性质的理解掌握和参加反应的物质质量数的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.

练习册系列答案
相关题目
6.关于人体吸入空气与呼吸排出的气体的叙述,正确的是( )
| A. | 呼出的气体与空气相比,氧气有明显减少,二氧化碳和水蒸气则有明显增加 | |
| B. | 空气与呼出的气体都是无色的气体,其成分完全相同 | |
| C. | 减少吸入空气中的氧气使转化为呼出的气体 | |
| D. | 吸入的空气中只有氧气,呼出的气体中只有二氧化碳和水蒸气 |
3.点燃下列混合气体,可能发生爆炸的是( )
| A. | 氢气和氦气 | B. | 氢气和二氧化碳 | C. | 氢气和氮气 | D. | 氢气和空气 |
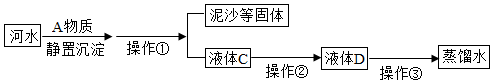
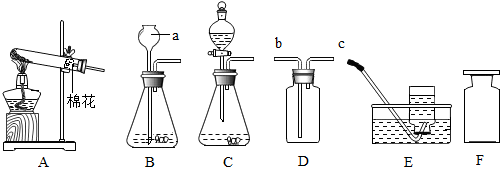
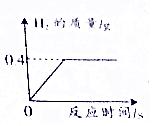 将20g Cu-Zn合金粉末投入一定足量的稀硫酸中,反应放出气体的质量与反应时间的关系如图所示.请计算:
将20g Cu-Zn合金粉末投入一定足量的稀硫酸中,反应放出气体的质量与反应时间的关系如图所示.请计算: