题目内容
结合图示回答问题.
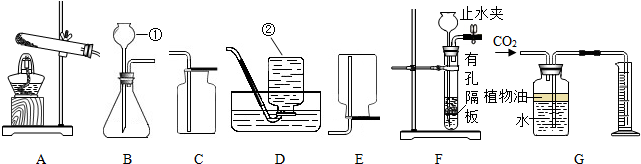
(1)写出图中标示的仪器名称:① ,② .
(2)实验室用KMnO4制取O2,应选用的发生装置为 (填字母序号,下同),收集装置可选用 ,写出该反应的化学方程式 .
(3)注射器与装置B相连可用于检查装置B的气密性,步骤如下:
①向锥形瓶中加入少量水至 .
②将注射器连接到装置B的导管口处.
③缓慢拉动注射器的活塞,观察到 ,说明装置B的气密性良好.
(4)实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是 ,图G所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是: ,植物油上方原有的空气对实验结果 (填“有”或“无”)明显影响.

(1)写出图中标示的仪器名称:①
(2)实验室用KMnO4制取O2,应选用的发生装置为
(3)注射器与装置B相连可用于检查装置B的气密性,步骤如下:
①向锥形瓶中加入少量水至
②将注射器连接到装置B的导管口处.
③缓慢拉动注射器的活塞,观察到
(4)实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是
考点:常用气体的发生装置和收集装置与选取方法,检查装置的气密性,实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(4)不同的实验装置,功能不同;
二氧化碳能够溶于水.
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(4)不同的实验装置,功能不同;
二氧化碳能够溶于水.
解答:解:(1)①是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品; ②是集气瓶,常用来收集气体.
故填:长颈漏斗;集气瓶.
(2)实验室用KMnO4制取氧气需要加热,应选用的发生装置为A装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用D装置收集;
该反应的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑.
故填:A;C或D;2KMnO4
K2MnO4+MnO2+O2↑.
(3)①向锥形瓶中加入少量水至浸没长颈漏斗末端;
②将注射器连接到装置B的导管口处;
③缓慢拉动注射器的活塞,观察到长颈漏斗末端出现气泡,说明装置B的气密性良好.
故填:浸没长颈漏斗末端;长颈漏斗末端出现气泡.
(4)实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是能使反应随时进行或停止;
其中在水面上放一层植物油的目的是防止二氧化碳溶于水;
植物油上方原有的空气对实验结果无明显影响,因为有多少体积的二氧化碳进入广口瓶中时,会有多少体积的水被排入量筒中,所以植物油上方原有的空气对实验结果无明显影响.
故填:能使反应随时进行或停止;防止二氧化碳溶于水;无.
故填:长颈漏斗;集气瓶.
(2)实验室用KMnO4制取氧气需要加热,应选用的发生装置为A装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用D装置收集;
该反应的化学方程式为:2KMnO4
| ||
故填:A;C或D;2KMnO4
| ||
(3)①向锥形瓶中加入少量水至浸没长颈漏斗末端;
②将注射器连接到装置B的导管口处;
③缓慢拉动注射器的活塞,观察到长颈漏斗末端出现气泡,说明装置B的气密性良好.
故填:浸没长颈漏斗末端;长颈漏斗末端出现气泡.
(4)实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是能使反应随时进行或停止;
其中在水面上放一层植物油的目的是防止二氧化碳溶于水;
植物油上方原有的空气对实验结果无明显影响,因为有多少体积的二氧化碳进入广口瓶中时,会有多少体积的水被排入量筒中,所以植物油上方原有的空气对实验结果无明显影响.
故填:能使反应随时进行或停止;防止二氧化碳溶于水;无.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
2008年6月14日是我国第三个“文化遗产日”.其制作过程主要属于化学变化( )
A、 永康锡艺 |
B、 浦江剪纸 |
C、 义乌米酒 |
D、 东阳木雕 |
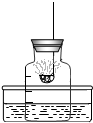 在“空气中氧气含量的测定”实验探究中,小明设计了如图所示实验装置,集气瓶下端为开口(即没有瓶底),上端瓶口有一带有燃烧匙的橡皮塞,瓶上带有刻度线,把集气瓶离水面的位置与橡皮塞之间的容积分成五等份.实验时把点燃的红磷立即插入集气瓶内,塞紧橡皮塞.回答下列问题:
在“空气中氧气含量的测定”实验探究中,小明设计了如图所示实验装置,集气瓶下端为开口(即没有瓶底),上端瓶口有一带有燃烧匙的橡皮塞,瓶上带有刻度线,把集气瓶离水面的位置与橡皮塞之间的容积分成五等份.实验时把点燃的红磷立即插入集气瓶内,塞紧橡皮塞.回答下列问题: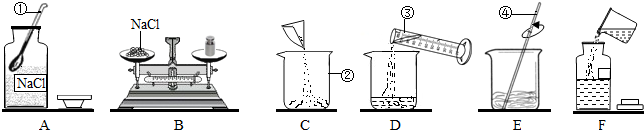
 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究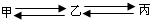 甲、乙、丙是初中化学常见的三种物质,在一定条件下它们之间的转换关系如图所示(部分物质及反应条件均已略去),其中甲、乙是组成元素相同的两种气体,且丙是常用的建筑材料.请回答:
甲、乙、丙是初中化学常见的三种物质,在一定条件下它们之间的转换关系如图所示(部分物质及反应条件均已略去),其中甲、乙是组成元素相同的两种气体,且丙是常用的建筑材料.请回答: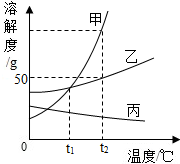 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题: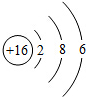 R元素的原子结构示意图如图所示,其原子的最外层电子数
R元素的原子结构示意图如图所示,其原子的最外层电子数