题目内容
15.元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:| 族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)请从上表中查出关于硅元素的一条信息:硅原子核内质子数为14(硅元素属于非金属元素等).
(3)第3横行(周期)中属于金属元素的是钠(或镁、铝)(填一种),该元素的离子与Cl-形成的化合物的化学式为NaCl(或MgCl2、AlCl3).
分析 (1)题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式.
(2)根据元素周期表中每一小方格中的信息分析;
(3)根据化合物的化学式的写法来分析.
解答 解:(1)①离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.表示多个离子在离子符号前面加数字,故酸离子符号为:S2-;故填:S2-
②由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故、三个钠原子可表示为:3Na.故填:3Na
③氩气是一种稀有气体,化学式直接用元素符号来表示,故填:Ar;
(2)元素周期表中每一小方格中左上角数字表示原子序数即核电荷数,符号表示元素符号,下方数字表示相对原子质量,因此关于硅元素的一条信息为硅的元素符号为Si,或:硅原子的核电荷数为14或硅原子的相对原子质量为28.09.故填:硅原子核内质子数为14(硅元素属于非金属元素等);
(3)第3周期中的金属元素有钠、镁、铝三种,在化合物中,钠元素显+1价,镁元素显+2价,铝元素显+3价,氯元素显-1价,故填:钠(或镁、铝);NaCl(或MgCl2、AlCl3)
点评 本题难度较小,考查学生灵活应用元素周期表的相关知识解答有关问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列物质敞口露置于空气中,质量不变的是( )
| A. | 氢氧化钙 | B. | 氯化钠 | C. | 生石灰 | D. | 浓盐酸 |
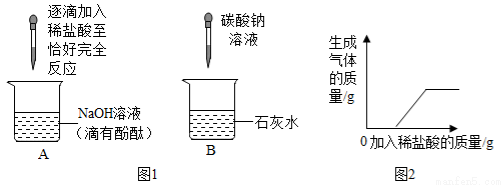
6.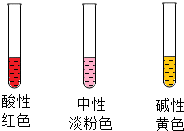 小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.
小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.
资料:
(1)纯碱的化学式为Na2CO3.
(2)将紫甘蓝汁滴入溶液A中,紫甘蓝汁显红色,则A溶液是饮水机清洁剂.
(3)将B溶液滴入A中,无明显现象,由此得出的结论是B是食盐水或石灰水.
(4)将C溶液滴入D、E中,均有沉淀产生,该过程的反应之一是(用化学方程式表示)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(5)为进一步区别D、E,小明试着向其溶液中分别通入CO2,观察到D中有沉淀产生,E中无明显现象,试推测D的成分并说明理由D为碳酸钠,CO2+H2O+Na2CO3=2NaHCO3碳酸氢钠的溶解度较小从而析出.
 小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.
小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.资料:
| 物质 | 碳酸钠 | 碳酸氢钠 |
| 20°C溶解度/g | 21.5 | 9.6 |
| 水溶液的pH | 11 | 9 |
(2)将紫甘蓝汁滴入溶液A中,紫甘蓝汁显红色,则A溶液是饮水机清洁剂.
(3)将B溶液滴入A中,无明显现象,由此得出的结论是B是食盐水或石灰水.
(4)将C溶液滴入D、E中,均有沉淀产生,该过程的反应之一是(用化学方程式表示)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(5)为进一步区别D、E,小明试着向其溶液中分别通入CO2,观察到D中有沉淀产生,E中无明显现象,试推测D的成分并说明理由D为碳酸钠,CO2+H2O+Na2CO3=2NaHCO3碳酸氢钠的溶解度较小从而析出.
7.某同学在实验室进行了木炭还原氧化铜的实验,实验步骤如下:
⑤为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究(注:该反应还原产物只有铜).
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
| 实验装置 | 实验步骤 | 分析 |
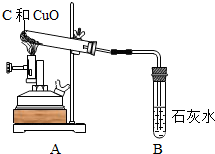 | ①检验装置气密性 | |
| ②把木炭和氧化铜的混合物放入试管,如左图所示连接实验装置 | 装置中存在的问题是B试管处不应该有橡皮塞 | |
| ③改进装置后,点燃酒精喷灯开始实验 | 装置B的作用是检验产物是否有二氧化碳 | |
| ④反应结束时,先将导管从装置B中撤出,再停止加热 | 目的是防止液体倒流引起试管炸裂 |
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
4.下列图示实验操作中,正确的是( )
| A. |  | B. |  | C. | 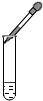 | D. | 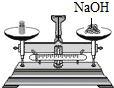 |
5.下列实验现象的描述不正确的是( )
| A. | 电解水时,正极产生氧气负极产生氢气 | |
| B. | 红磷在空气中燃烧,产生大量白烟 | |
| C. | 镁和稀盐酸反应产生无色气体,放出热量 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 |