题目内容
12.回答下列与金属有关的问题.(1)铝合金和纯铝,硬度较大的是铝合金;
(2)工业上,把赤铁矿冶炼成铁的主要反应原理是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,其中Fe2O3发生了还原反应;
(3)比较Mn、Pd(钯)、Cu三种金属的活动性顺序
①将Mn片、Pd片分别加入到稀盐酸中,Mn片表面有气泡产生,Pd片没有变化.根据上述实验现象,得出的结论是Mn的活泼性比Pd强;
②要确切得出这三种金属的活动性顺序,还需将Pd片加入到硫酸铜溶液中,观察现象.
分析 (1)根据合金的特点分析;
(2)根据氧化还原反应的实质进行分析;
(3)根据金属活动顺序表中Mn、Pd(钯)、Cu的金属活动性强弱去分析解答.
解答 解:(1)一般说来合金的硬度一般比各成分金属大,合金的熔点一般低于组成它的成分金属的熔点.故填:铝合金;
(2)根据高炉炼铁的原理:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2可知,在此反应中一氧化碳得氧发生了氧化反应,是还原剂;Fe2O3失氧发生了还原反应,是氧化剂;故填:Fe2O3
(3)①将Mn片、Pd片分别加入到稀盐酸中,Mn片表面有气泡产生,Pd片没有变化,说明Mn的活泼性比Pd强.②要确切得出这三种金属的活动性顺序,还需将Pd片加入到铜盐中,如硫酸铜溶液中,观察Pd片表面是否有红色的金属铜出现,如有,说明Pd的活泼性比铜强,没有,则说明Pd的活泼性不如铜;
故答案为:①Mn的活泼性比Pd强;②硫酸铜;
点评 本题考查合金的性质,氧化还原反应,金属的活泼性比较等,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.某化学反应的微观过程如图所示,则下列说法正确的是( )


| A. | 反应前后含氢元素的化合物有2种 | B. | 反应前后原子的种类发生了改变 | ||
| C. | 反应前后各元素化合价没有改变 | D. | 反应前后分子个数没有发生改变 |
3.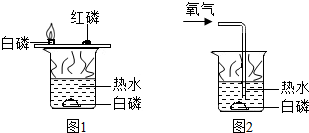 下列所示的一级实验可用于研究燃烧条件,下列说法正确的是( )
下列所示的一级实验可用于研究燃烧条件,下列说法正确的是( )
 下列所示的一级实验可用于研究燃烧条件,下列说法正确的是( )
下列所示的一级实验可用于研究燃烧条件,下列说法正确的是( )| A. | 此组实验烧杯中的热水只起提高温度的作用 | |
| B. | 图1和图2中水下白磷对比说明燃烧必须要用氧气 | |
| C. | 图1中铜片上的白磷和红磷对比说明燃烧必须有氧气 | |
| D. | 图1中铜片上的红磷和水下的白磷对比说明燃烧必须达到可燃物的着火点 |
7.下列有关催化剂的说法正确的是( )
| A. | 催化剂都能够加快化学反应速率 | |
| B. | 催化剂在化学反应中能增加生成物的质量 | |
| C. | 催化剂在化学反应前后质量和化学性质不变 | |
| D. | 二氧化锰是所有化学反应的催化剂 |
11.把500L空气压缩到1L的钢瓶中,是因为( )
| A. | 分子变小了 | B. | 分子间的间隔变小了 | ||
| C. | 分子静止了 | D. | 分子破裂成了原子 |
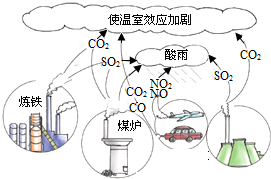 请仔细观察图,回答有关问题.
请仔细观察图,回答有关问题.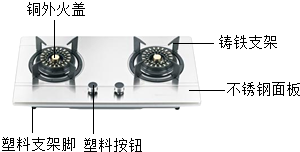 我国大多数城镇居民已从最早的柴煤灶改为了现在的燃气灶,燃料从煤炭到现在的天然气,更加安全而且成本也更低.如图是某品牌燃气灶结构图.请你回答下列问题.
我国大多数城镇居民已从最早的柴煤灶改为了现在的燃气灶,燃料从煤炭到现在的天然气,更加安全而且成本也更低.如图是某品牌燃气灶结构图.请你回答下列问题.