题目内容
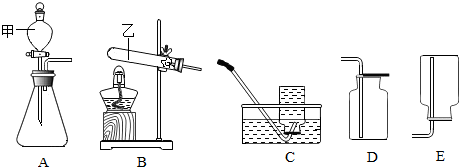
13.现有下列如图1A、B、C、D、E五种实验装置,根据题意,将装置的序号填入下列空格中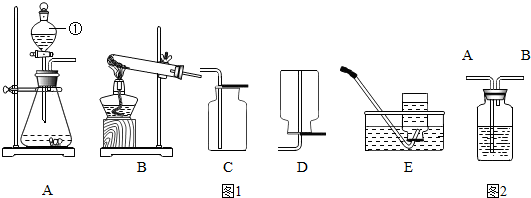
(1)写出指定仪器的名称:①分液漏斗;
(2)用高锰酸钾制取氧气,发生装置选用:(填序号)B、写出用高锰酸钾制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)若要收集比较纯净的氧气,应选用(填序号)E
(4)用过氧化氢溶液制取氧气,发生装置选用(填序号)A 写出用过氧化氢溶液制取氧气化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2).;用C装置收集氧气时验满方法是可将带火星的木条伸入集气瓶内,若木条复燃说明是氧气.用此方法制氧气和用高锰酸钾制氧气相比,其优点是(写一条)不需加热等.
(5)氨气无色、有刺激性气味,极易溶于水,密度比空气小;实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气.则发生装置应用(填序号)B; 收集氨气装置最好用(填序号)D
(6)图2是化学中“有名”的装置,有如下用途:医院里给病人输氧,为了给氧气加湿和观察氧气的输出速度,也可以在氧气瓶和病人之间连接该装置,在集气瓶装半瓶水,将A端接氧气钢瓶,通过观察气泡产生的快慢就知道氧气的输出速度.
分析 (1)根据常用仪器的名称和用途分析回答;
(2)根据用高锰酸钾制取氧气的反应物的状态及反应条件确定发生装置;根据反应的原理写出反应的化学方程式;
(3)根据用排水法收集的气体较为纯净分析回答;
(4)根据用过氧化氢溶液制取氧气反应物的状态及反应条件确定发生装置;根据反应的原理写出反应的化学方程式;对比两种制取氧气的原理、装置等,分析优点.
(5)根据实验室制取氨气的反应物的状态及反应条件确定发生装置,根据氨气的收集方法确定收集装置;
(6)根据装置的特点、应用分析分析回答.
解答 解:(1)由图示可知,仪器①的名称是分液漏斗;
(2)用高锰酸钾制取氧气,属于加热固体制取气体,发生装置选用B,用高锰酸钾制取氧气的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)若要收集比较纯净的氧气,应选用排水法收集,应选用的装置E;
(4)用过氧化氢溶液制取氧气,属于固液常温下反应,发生装置选用A,用过氧化氢溶液制取氧气化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2;由于氧气具有助燃性,用C装置收集氧气时验满方法是:可将带火星的木条伸入集气瓶内,若木条复燃说明是氧气.用此方法制氧气和用高锰酸钾制氧气相比,其优点是不需加热、操作简便等.
(5)实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气.属于加热固体制取气体,则发生装置应用B; 氨气无色、有刺激性气味,极易溶于水,密度比空气小;应用向上排气法收集,收集氨气装置最好用D.
(6)给氧气加湿,氧气从钢瓶中出来要通过水中,所以A端接氧气瓶,通过观察气泡产生的快慢就知道氧气的输出速度.
故答为:(1)分液漏斗;(2)B、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(3)E;(4)A,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2;由于氧气具有助燃性,可将带火星的木条伸入集气瓶内,若木条复燃说明是氧气.不需加热、操作简便等.(5)B;D.(6)A,气泡产生的快慢.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 名校课堂系列答案
名校课堂系列答案| A. | 铁熔化成铁水 | B. | 酒精挥发 | C. | 蒸气锅炉爆炸 | D. | 蜡烛燃烧 |
【实验过程】
甲组实验方案:将四瓶溶液标号分别为1、2、3、4,只利用紫色石蕊溶液进行实验.

乙组实验方案:不用其他试剂进行实验.
| 实验操作 | 实验现象 | 实验结论 |
| 任取三种溶液于三支试管中,分别滴加第四种溶液 | ①一支试管中有气泡放出,其余两支试管中无明显变化 | ①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出,其余两支试管中溶液无明显变化 | ③第四种为Na2CO3溶液 | |
| ④三支试管中溶液均无明显变化 | ②第四种为NaOH溶液 |
经过交流后,发现实验结论②(填序号)是不正确的;若该结论作正确,对应的实验现象应是一支试管中有气泡放出、一支试管中有白色沉淀析出、一支试管中无明显现象.
丙组实验方案:将四种溶液编号为1、2、3、4,不用其他试剂进行实验.

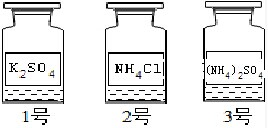
丁组实验方案:将四种溶液重新编号为1、2、3、4,各取少量溶液于四支试管中,分别加热.1中产生刺激性气味,2、3无明显变化,4中溶液变浑浊.冷却后,再取少量澄清4号溶液滴入2、3中,2号溶液无明显变化,3号溶液变浑浊.
通过以上实验,鉴别出号溶液是稀盐酸;加热4号溶液变浑浊的原因是氢氧化钙的溶解度随温度的升高而降低,因此石灰水加热时会有氢氧化钙的析出.
 如图所示是某小组同学做铁丝在氧气中燃烧的实验.请回答问题:
如图所示是某小组同学做铁丝在氧气中燃烧的实验.请回答问题: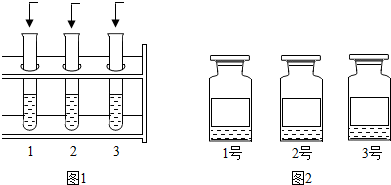
 .
.