题目内容
7.某化学兴趣小组进行铁生锈的实验探究活动.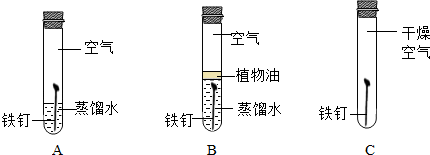
【探究一】铁生锈的条件
(1)该兴趣小组将洁净无锈的铁钉分别置于上图所示装置中,经过一段时间观察A,(填装置序号)装置中出现了明显的锈迹.
他们的结论:铁生锈是因为铁与空气中的氧气和水蒸气等发生了化学反应.
(2)甲同学提出了疑问:空气中的氮气、二氧化碳没有参与铁的生锈过程吗?请设计实验为甲同学释疑.将A装置中的氧气换作氮气或二氧化碳,观察并记录现象即可证明.
【探究二】影响铁生锈速率快慢的因素
乙同学说:妈妈常说菜刀沾有盐水生锈更快.这种说法对吗?同学广泛查阅资料.
资料一:导电性强的溶液都可加速铁的生锈.
资料二:海上航行的轮船在与海水接触的部分镶嵌一锌块,能有效降低钢材被腐蚀的速率.
(3)将上述A装置中的蒸馏水改为下列液体中的A,可使铁生锈的速率加快.
A.硫酸钠溶液 B.无水乙醇 C.蔗糖溶液
(4)一些建筑的大门刷上了一层银白色的金属,你认为该金属可能是C.
A.银粉 B.铜粉 C.镁粉
(5)写出一种防止铁生锈的方法刷油漆.
分析 (1)根据铁生锈的条件解答;
(2)控制变量设计实验;
(3)根据所给资料一分析解答;
(4)根据防锈原理解答;
(5)根据防锈方法解答.
解答 解:(1)铁生锈的条件是铁与空气中的水分和氧气共同作用的结果,A中铁钉满足铁生锈的条件,一段时间后会出现明显的锈迹.
(2)将A装置中的氧气换做氮气或二氧化碳就可验证空气中氮气或二氧化碳有没有参加铁生锈的反应.
(3)因为导电的溶液可加速铁的生锈,硫酸钠溶液中含有钠离子和硫酸根离子,如果把蒸馏水换为硫酸钠溶液可使铁生锈速率加快.
(4)大门上刷一层银白色金属,该金属可能是镁,因为镁在空气能形成一层致密坚固的氧化镁薄膜,隔绝水分和氧气,起到防锈作用.
(5)铁制品防锈的方法有涂保护层,刷油漆等.
故答案为:
(1)A;氧气和水蒸气;
(2)将A装置中的氧气换作氮气或二氧化碳;
(3)A;
(4)C;
(5)刷油漆.
点评 该题的难点是根据所给的资料信息提炼出有用的信息并运用到题目中解题.如资料一:导电的溶液可加速铁生锈,这里就要知道什么样的溶液易导电,一般是溶液电离出阴阳离子的溶液,如氯化钠溶液、硫酸钠溶液等;资料二:轮船上镶嵌锌块,防止钢的腐蚀,说明活泼的金属更易腐蚀.提炼出这些信息,解题就不难了.

练习册系列答案
相关题目
10.下列四个化学反应中,符合此漫画情景的是( )
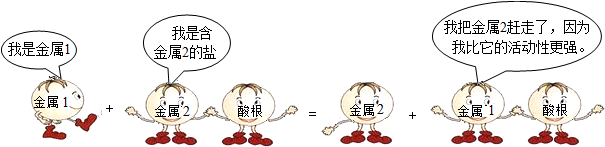

| A. | Cu+2AgCl═Ag+CuCl2 | B. | Fe+H2S04═FeS04+H2↑ | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H20 | D. | Fe+CuS04═FeS04+Cu |
15.下列实验设计能达到实验目的是
( )
| 序号 | 实验目的 | 实验方案 |
| A | 证明某物质中一定含有CO32- | 加入稀盐酸有气泡产生 |
| B | 制取Ag | 用Fe与AgCl反应 |
| C | 区分氧化钙与碳酸钙 | 取样品,加入适量水 |
| D | 除去K2S04溶液中的K0H | 加入适量稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
12.归纳和类推是学习化学常用的思维方法.现有下列类推结果,其中错误的是( )
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
④离子是带电的原子或原子团,所以带电的微粒一定是离子.
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
④离子是带电的原子或原子团,所以带电的微粒一定是离子.
| A. | 只有① | B. | 只有①②③ | C. | 只有②③④ | D. | 只有①②③④ |
16.如图各组变化中,每个转化在一定条件下均能一步实现的是( )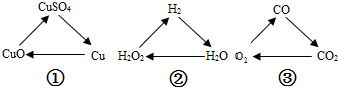

| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
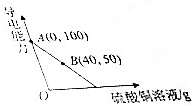 已知向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系.
已知向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系.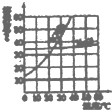 根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.
根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.