题目内容
向硝酸银、硝酸亚铁的混合溶液中加入一定量的锌粉,反应停止后过滤,得到滤渣A和滤液B.向A中加入稀硫酸,A部分溶解且有气泡产生.根据以上事实用化学用语填空:
(1)A中一定含有Ag和 ;
(2)B中一定有的金属离子是 ,可能有的金属离子是 .
(1)A中一定含有Ag和
(2)B中一定有的金属离子是
考点:金属的化学性质
专题:金属与金属材料
分析:根据在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,向滤渣A中加入稀硫酸,有气泡冒出,说明滤渣中含有能与酸反应的金属,然后根据题中的现象进行分析解答.
解答:解:(1)加入一定质量的锌粉时先置换活动性最弱的金属,然后在置换较强的.
硝酸银、硝酸亚铁的混合溶液中加入一定量的锌粉,可能会发生:锌能与硝酸银反应生成硝酸锌和银,锌能与硝酸亚铁反应生成硝酸锌和铁,银均不能与稀盐酸反应,铁、锌能与稀盐酸反应,所以充分反应后过滤,向滤渣A中加入稀盐酸,有气泡冒出,说明滤渣中含有能与酸反应的活泼金属,则滤出的固体中则一定含有铁,可能含有锌,则滤渣A中一定有Ag、Fe;
(2)由于可能是置换完铁后锌还有剩余,B中一定含有的金属离子是:Zn2+,可能含有的金属离子是:Fe2+.
故答案为:(1)Fe;
(2)Zn2+,Fe2+.
硝酸银、硝酸亚铁的混合溶液中加入一定量的锌粉,可能会发生:锌能与硝酸银反应生成硝酸锌和银,锌能与硝酸亚铁反应生成硝酸锌和铁,银均不能与稀盐酸反应,铁、锌能与稀盐酸反应,所以充分反应后过滤,向滤渣A中加入稀盐酸,有气泡冒出,说明滤渣中含有能与酸反应的活泼金属,则滤出的固体中则一定含有铁,可能含有锌,则滤渣A中一定有Ag、Fe;
(2)由于可能是置换完铁后锌还有剩余,B中一定含有的金属离子是:Zn2+,可能含有的金属离子是:Fe2+.
故答案为:(1)Fe;
(2)Zn2+,Fe2+.
点评:本题难度不是很大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
相关题目
下列说法正确的是( )
| A、测定pH最简单的方法是使用pH试纸 |
| B、硫酸有腐蚀性,盐酸没有腐蚀性 |
| C、用PH试纸测得某酸溶液PH为3.5 |
| D、pH为1的硫酸溶液比pH为1的盐酸溶液酸性强 |
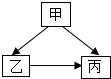 如图所示为甲、乙、丙三种物质的化学变化转化关系.
如图所示为甲、乙、丙三种物质的化学变化转化关系.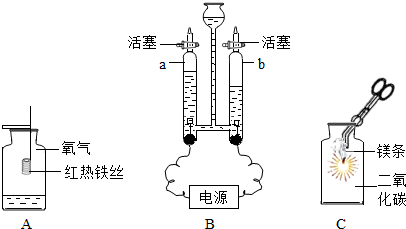
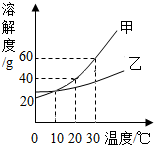 如图是甲、乙两物质的溶解度曲线图,据图回答下列问题
如图是甲、乙两物质的溶解度曲线图,据图回答下列问题 如图1是一种自发热“取暖袋”外包装的图片.该“取暖袋”中主要成分有铁粉、炭粉、氯化钠、蛭石、水等.某兴趣小组将“取暖袋”剪开口,安放在如图2的装置中.
如图1是一种自发热“取暖袋”外包装的图片.该“取暖袋”中主要成分有铁粉、炭粉、氯化钠、蛭石、水等.某兴趣小组将“取暖袋”剪开口,安放在如图2的装置中.