题目内容
11.化学是研究物质的组成、结构、性质、用途及其变化规律的基础自然科学,请回答下列问题:(1)从组成角度看:硫酸是重要的化工原料,硫酸是由H、S、O三种元素组成的.
(2)从微粒角度看:硫酸是由H+(填离子符号)和SO42-构成的.
(3)从性质角度看:稀硫酸溶液可使石蕊试液显红色,说明其具有酸性.请写
出其与氢氧化钠反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
(4)从变化角度看:铅酸蓄电池内的物质是二氧化铅(PbO2)、海绵铅和硫酸溶液,
充电时反应生成硫酸铅(PbSO4)和另一种物质X,反应的化学方程式为:PbO2+Pb+2H2SO4═2PbSO4+2X.
①则X的化学式为H2O;
②该过程是将电能转化为化学能.
(5)硫酸是一种重要的化工原料,请写出其一种用途除锈.
分析 (1)根据物质是由元素组成的进行解答;
(2)根据从微粒角度看硫酸是由氢离子和硫酸根离子构成进行解答;
(3)稀硫酸溶液可使石蕊试液显红色,说明其具有酸性;
(4)根据反应前后原子个数和种类不变进行分析解答;
(5)硫酸是一种重要的化工原料,可用于金属除锈.
解答 解:(1)从组成角度看,硫酸由H、S、O三种元素组成;
(2)从微粒角度看硫酸是由氢离子和硫酸根离子构成;
(3)稀硫酸溶液可使石蕊试液显红色,说明其具有酸性,与氢氧化钠反应的化学方程式:H2SO4+2NaOH=Na2SO4+2H2O;
(4)反应前后原子个数和种类不变,则X的化学式为H2O;该过程是将电能转化为化学能;
(5)硫酸是一种重要的化工原料,可用于金属除锈.
故答案为:(1)H、S、O三种元素;
(2)H+;
(3)酸; H2SO4+2NaOH=Na2SO4+2H2O;
(4)①H2O;②化学;
(5)除锈.
点评 本题考查了常见物质的组成、结构、性质及变化规律,要加强基础知识的记忆.

练习册系列答案
相关题目
1.某品牌厨房清洁剂的主要成分是氢氧化钠,其俗称为( )
| A. | 纯碱 | B. | 小苏打 | C. | 烧碱 | D. | 生石灰 |
2.下列依据实验目的所设计的实验操作中,合理的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验二氧化碳 | 将气体通入紫色石蕊溶液中 |
| B | 鉴别氮气和二氧化碳 | 将燃着的木条伸人集气瓶中 |
| C | 测定溶液的pH | 用胶头滴管吸待测试液滴在湿润的pH试纸上 |
| D | 干燥氧气 | 把氧气通过装有浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
19.下列说法正确的是( )
| A. | 蓄电池充电是电能转化成化学能 | B. | 合金是合成材料 | ||
| C. | 食用加碘盐可预防贫血病 | D. | 绿色食品不含任何化学物质 |
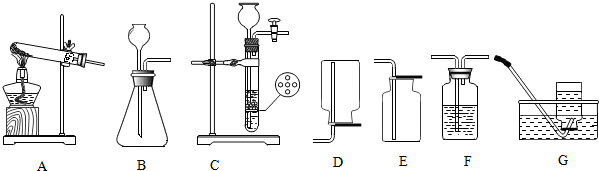
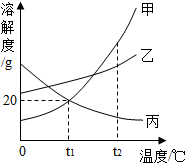 三种物质的溶解度曲线如图所示,回答问题:
三种物质的溶解度曲线如图所示,回答问题: