题目内容
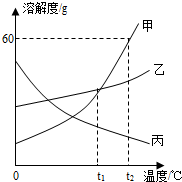 (2012?徐州)如图是三种物质的溶解度曲线,下列说法正确的是( )
(2012?徐州)如图是三种物质的溶解度曲线,下列说法正确的是( )分析:A、根据丙物质的溶解度是随着温度的升高而减小分析;
B、根据t1℃时甲、乙两物质的溶解度曲线在一交叉点上分析;
C、根据t2℃时甲物质溶解度是60g分析;
D、根据温度低于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数小分析;
B、根据t1℃时甲、乙两物质的溶解度曲线在一交叉点上分析;
C、根据t2℃时甲物质溶解度是60g分析;
D、根据温度低于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数小分析;
解答:解:A、丙物质的溶解度是随着温度的升高而减小,所以丙物质的饱和溶液升温后,会有晶体析出,还是饱和溶液,故A错误;
B、t1℃时甲、乙两物质的溶解度曲线在一交叉点上,所以溶解度相等,故B正确;
C、t2℃时甲物质溶解度是60g,将70g甲物质加入100g水中,可得到160g溶液,故C错误;
D、温度低于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数小,温度高于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数大,故D错误;
故选B.
B、t1℃时甲、乙两物质的溶解度曲线在一交叉点上,所以溶解度相等,故B正确;
C、t2℃时甲物质溶解度是60g,将70g甲物质加入100g水中,可得到160g溶液,故C错误;
D、温度低于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数小,温度高于t1℃时,甲物质的溶质质量分数比乙物质的溶质质量分数大,故D错误;
故选B.
点评:掌握固体溶解度曲线的变化趋势及其作用;了解溶质的质量分数、溶解性和溶解度的关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
