题目内容
2.实验室用19.6%的稀硫酸处理一定量含有氢氧化钠的废液,共消耗稀硫酸50g,处理后溶液呈中性,计算这一定量的废液中含氢氧化钠的质量是多少?分析 根据处理后溶液呈中性说明两种溶液恰好完全反应,利用溶液的溶质质量分数计算氢稀硫酸中溶质质量,然后根据反应的化学方程式计算氢氧化钠的质量解答.
解答 解:50g19.6%的稀硫酸中溶质质量=50g×19.6%=9.8g
设这一定量的废液中含氢氧化钠的质量是x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
x 9.8g
$\frac{80}{x}=\frac{98}{9.8g}$
x=8g
答案:这一定量的废液中含氢氧化钠的质量是8g.
点评 根据溶液的溶质质量分数首先计算出溶液中溶质质量,然后利用化学方程式进行计算.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
12.下列物质露置在潮湿的空气中,质量都会变大,其中不涉及到化学变化的是( )
| A. | 浓硫酸 | B. | 氢氧化钠固体 | C. | 生石灰 | D. | 铁粉 |
13.下列关于“燃烧和灭火”的叙述正确的是( )
| A. | 炒菜时油锅着火,立即盖上锅盖 | B. | 家用电器着火,立即用水扑灭 | ||
| C. | 只有含碳元素的物质才能燃烧 | D. | 可燃物与氧气接触,就能燃烧 |
10.春天郊游,禁止乱扔烟头,以防发生火灾,你认为禁止乱扔烟头是因为( )
| A. | 烟头提供了可燃物 | B. | 烟头会改变可燃物着火点 | ||
| C. | 烟头会使可燃物温度达到着火点 | D. | 烟头的着火点较低 |
7.材料与人类生活息息相关,下列物质与所用的材料相对应关系不正确的是( )
| A. | 纯棉毛巾-合成纤维 | B. | 汽车轮胎-合成橡胶 | ||
| C. | 食品袋-塑料 | D. | 不锈钢餐具-铁合金 |
11.下列是小刚“配制50g溶质质量分数为8%的氢氧化钠溶液”的实验过程,其中正确的是( )
| A. | 计算需要氢氧化钠4g、水46g | |
| B. | 将氢氧化钠放在托盘天平左盘的纸上称量 | |
| C. | 将称取的氢氧化钠放入量筒中溶解 | |
| D. | 将配制好的溶液转移一半后,小刚认为剩余溶液溶质质量分数为4% |
9. 20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
 20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )
20l6年1月5日,南昌西汉海昏侯墓主棺使用泡沫材料完成套箱打包.已知制作泡沫材料的原料之一是环氧乙烷 (C2H4O),则下列关于环氧乙烷的说法正确的是( )| A. | 环氧乙烷由三个元素组成 | |
| B. | 环氧乙烷分子中含有7个原子 | |
| C. | 环氧乙烷中碳元素和氢元素的质量比为1:2 | |
| D. | 环氧乙烷的相对分子质量为44,其中碳元素的质量分数最大 |
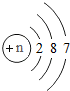 是某种元素原子结构示意图,该原子的核电荷数n为17,最外层有7个电子,在化学反应中,这种原子容易得到电子.
是某种元素原子结构示意图,该原子的核电荷数n为17,最外层有7个电子,在化学反应中,这种原子容易得到电子.