题目内容
7. 为测定空气的成分,设计了如图实验装置进行实验,加入少量水后,将集气瓶体积分成5等份.按要求填空:
为测定空气的成分,设计了如图实验装置进行实验,加入少量水后,将集气瓶体积分成5等份.按要求填空:(1)将燃烧匙中过量的红磷点燃后放入集气瓶中,能观察到的现象是剧烈燃烧,产生大量白烟,此实验说明氮气的物理性质是不溶于水,化学性质是不能燃烧,不支持燃烧
(2)若装置不漏气,冷却后打开弹簧夹,进入的水大约达到集气瓶体积的五分之一.
(3)某些同学认为,用木炭代替红磷也可以得出空气中氧气体积含量的结果,结果没有成功.请你分析不能成功的原因木炭燃烧虽然消耗了氧气,但同时生成了二氧化碳气体,装置内气压变化不明显.
分析 红磷在空气中燃烧时很剧烈,产生大量白烟,放出大量的热,生成白色固体;
氧气约占空气总体积的五分之一;
氮气不溶于水,不能燃烧,不支持燃烧;
木炭燃烧生成二氧化碳气体.
解答 解:(1)将燃烧匙中过量的红磷点燃后放入集气瓶中,能观察到的现象是剧烈燃烧,产生大量白烟,此实验说明氮气的物理性质是不溶于水,化学性质是不能燃烧,不支持燃烧.
故填:剧烈燃烧,产生大量白烟;不溶于水;不能燃烧,不支持燃烧.
(2)若装置不漏气,冷却后打开弹簧夹,进入的水大约达到集气瓶体积的五分之一.
故填:五分之一.
(3)因为木炭燃烧虽然消耗了氧气,但同时生成了二氧化碳气体,装置内气压变化不明显,水不能进入集气瓶,从而导致无法测定空气中氧气的含量.
故填:木炭燃烧虽然消耗了氧气,但同时生成了二氧化碳气体,装置内气压变化不明显.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
15.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,请写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成份是碳酸钙.
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3
猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验证明】
【反思与拓展】
(1)向CaH2和足量水反应后的溶液加入NH4Cl溶液,产生的气体是氧气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成份是碳酸钙.
【提出问题】滤液中溶质的成份是什么?
【猜想与假设】
猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3
猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验证明】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | Ⅰ:没有产生沉淀 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | Ⅱ:产生气泡 | 猜想三成立 |
(1)向CaH2和足量水反应后的溶液加入NH4Cl溶液,产生的气体是氧气、氨气.
(2)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.
15.下列物质属于气体并有刺激性气味的是( )
| A. | CO2 | B. | H2O | C. | NH3 | D. | NH4HCO3 |
2.1克下列物质中含有原子个数最多的是( )
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 铁 | D. | 一氧化碳 |
19.下列对课本中相关实验的分析不正确的是( )
| A. | 硫燃烧产生有害的气体,该实验可用水吸收有害气体 | |
| B. | 点燃氢气前一定要检验氢气的纯度 | |
| C. | 通过分离液态空气得到氮气和氧气的过程,属于化学变化 | |
| D. | 二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气 |
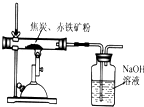 为了测定某赤铁矿中氧化铁(Fe2O3)的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).
为了测定某赤铁矿中氧化铁(Fe2O3)的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).