题目内容
1.实验室用双氧水和二氧化锰共100克制氧气,充分反应后,称得试管内剩余物质84克,求:(1)过氧化氢中氧、氢元素质量比
(2)生成氧气质量是16g
(3)过氧化氢的质量是多少?
分析 (1)根据化学式求算对应元素的质量比,在化合物中元素的质量比等于相对原子质量乘以原子个数之比;
(2)根据质量守恒定律可知生成的氧气的质量;
(3)根据氧气的质量和对应的化学方程式求算过氧化氢的质量.
解答 解:
(1)过氧化氢(H2O2)中氧元素和氢元素的质量比为(16×2):(1×2)=16:1;
(2)根据质量守恒定律可得,生成的氧气的质量为100g-84g=16g;
(3)设生成16g氧气需要的过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 16g
$\frac{68}{32}$=$\frac{x}{16g}$
x=34g
答:(1)过氧化氢中氧、氢元素质量比16:1;
(2)生成氧气质量是 16g.
(3)过氧化氢的质量是34g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
11.对下列化学用语中“2”的说法不正确的是( )
①2CO ②2N ③$\stackrel{+2}{Cu}$O ④2Na+ ⑤Mg2+ ⑥H2O.
①2CO ②2N ③$\stackrel{+2}{Cu}$O ④2Na+ ⑤Mg2+ ⑥H2O.
| A. | ①表示分子个数,③表示元素的化合价 | |
| B. | ②④表示原子个数 | |
| C. | ⑤表示离子所带电荷数 | |
| D. | ⑥表示一个分子中所含该原子个数 |
16.甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )
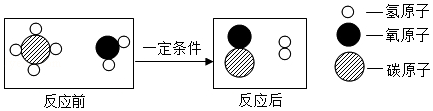

| A. | 反应前后各元素的化合价均不变 | |
| B. | 水煤气的成分是一氧化碳和氢气 | |
| C. | 该反应中含氢元素的化合物有3种 | |
| D. | 该反应的化学方程式中一氧化碳和氢气的计量数之比为1:1 |
10.下列实验操作正确的是( )
| A. |  测溶液pH | B. |  闻气体气味 | C. | 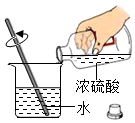 稀释浓硫酸 | D. |  点燃酒精灯 |
