题目内容
2. 如图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的$\frac{1}{1836}$,故原子的质量几乎都集中在原子核上.
如图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的$\frac{1}{1836}$,故原子的质量几乎都集中在原子核上.若用r、m分别表示微粒的半径和质量,以“<”或“>”或“≈”填空.
(1)m(Na)≈m(Na+)
(2)r(Cl)<r(Cl-)
(3)r(Na)>r(Cl)
(3)r(Na+)<r(Cl-)
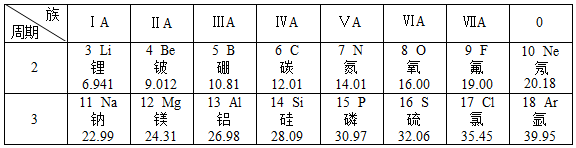
分析 根据元素周期律:同周期的元素一般满足从左往右半径依次减小,因为半径越小,对电子的吸附能力就越强,外围的电子数就越多;看离子核外电子层数,层数越多离子半径越大,进行解答.
解答 解:(1)1个电子的质量大约为1个质子或中子质量的$\frac{1}{1836}$,故原子的质量几乎都集中在原子核上,所以
m(Na)≈m(Na+); 故答案为:≈;
(2)因为Cl离子比Cl原子多了1个电子,所以Cl离子的半径大于Cl原子的半径;r(Cl)<r(Cl-);故答案为:<;
(3)根据同周期的元素一般满足从左往右半径依次减小,可知:r(Na)>r(Cl); 故答案为:>;
(4)离子半径比较:第一先看离子核外电子层数,层数越多离子半径越大,第二电子层数相同,看核电荷数核电荷数越大对外界电子的吸引力越大,离子半径反而越小.Na+只有两层电子层,Cl-有三层,因此Cl->Na+,可知:r(Na+)<r(Cl-).故答案为:<.
答案:
(1)≈;(2)<;(3)>;(4)<.
点评 本题考查学生对元素周期律:同周期的元素一般满足从左往右半径依次减小,进行解分析解题的能力.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
16.塑化剂是一种化工原料,属于致癌物质,不能用于食品添加剂.其最常见的品种是DEHP.
下列关于DEHP(化学式为C24H38O4)的说法正确的是( )
下列关于DEHP(化学式为C24H38O4)的说法正确的是( )
| A. | 碳、氢、氧三种元素质量比为24:38:4 | |
| B. | 氢元素的质量分数最小 | |
| C. | 属于氧化物 | |
| D. | 完全燃烧后可能生成二氧化硫气体污染环境 |
10.托盘天平使用正确是( )
| A. | 砝码用镊子取用 | B. | 右盘放药品 | ||
| C. | 药品直接放托盘 | D. | 某同学称取了6.85g药品 |
17. 如图所示,打开止水夹,将液体A滴人试管②中与固体B接触.若试管①中的导管口有气泡产生,则液体A和固体B的组合可能是下列中的( )
如图所示,打开止水夹,将液体A滴人试管②中与固体B接触.若试管①中的导管口有气泡产生,则液体A和固体B的组合可能是下列中的( )
 如图所示,打开止水夹,将液体A滴人试管②中与固体B接触.若试管①中的导管口有气泡产生,则液体A和固体B的组合可能是下列中的( )
如图所示,打开止水夹,将液体A滴人试管②中与固体B接触.若试管①中的导管口有气泡产生,则液体A和固体B的组合可能是下列中的( )| A. | 水和二氧化锰 | B. | 水和食盐 | C. | 稀盐酸和大理石 | D. | 水和白糖 |
12.镁条能在空气中燃烧,属于镁条的( )
| A. | 物理变化 | B. | 化学变化 | C. | 物理性质 | D. | 化学性质 |