题目内容
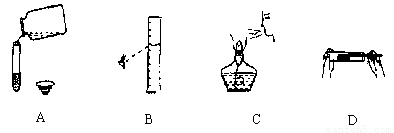
(8分)取47.4g高锰酸钾,加热一段时间后停止,剩余固体质量为44.2g.计算:
(1)反应后生成氧气的质量为______g.
(2)参加反应的高锰酸钾的质量.
(3)剩余固体中氧元素的质量为______g.
(1) 3.2g;(2) 31.6g;(3)16g.
【解析】
试题分析:
(1)反后固体质量减少的量就是生成的氧气的质量,所以生成的氧气的质量为47.4g-44.2g=3.2g;
(2)设参加反应的高锰酸钾的质量为X.
2KMnO4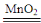 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
32
X 3.2g
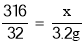
X=31.6g
答:参加反应的高锰酸钾的质量为31.6g.
(3)原高锰酸钾中氧元素的质量减去生成的氧气的质量即是剩余固体中的氧元素的质量,所以剩余固体中氧元素的质量为
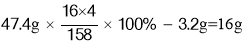
考点:根据方程式的计算;物质中某元素的质量分数的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下表列出了除去物质中少量杂质的方法,其中错误的是
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | CO2 | CO | 将气体点燃 |
B | N2 | O2 | 通过灼热的铜网 |
C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
D | FeCl2 | CuCl2 | 加入过量的铁粉,过滤 |
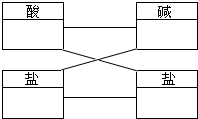 从你最熟悉的酸、碱、盐中,任意选出四种物质,使其符合图中的关系,图中连线的物质间均能发生化学反应,请将物质的化学式填在相应的方框内.
从你最熟悉的酸、碱、盐中,任意选出四种物质,使其符合图中的关系,图中连线的物质间均能发生化学反应,请将物质的化学式填在相应的方框内.