题目内容
现有9.3g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3.在室温下,将该混合物与50g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为57.1g,则原固体混合物中含有钠元素的质量为下列的( )
|
| A. | 1.15g | B. | 2.3g | C. | 4.6g | D. | 6.9g |
| 根据化学反应方程式的计算;化合物中某元素的质量计算. | |
| 专题: | 有关化学方程式的计算. |
| 分析: | 根据质量守恒定律可以计算出二氧化碳的质量,然后由生成气体二氧化碳的质量根据碳酸钠与硫酸反应的化学方程式,计算混合物中碳酸钠质量,进而求出氢氧化钠的质量,利用纯净物种某一元素的质量=纯净物的质量×元素在化合物中的质量分数. |
| 解答: | 解: 生成氧气的质量为:9.3g+50g﹣57.1g=2.2g; 设混合物中碳酸钠的质量为x, Na2CO3+H2SO4═Na2SO4+CO2↑+H2O 106 44 x 2.2g
x=5.3g NaOH的质量是9.3g﹣5.3g=4g 5.3gNa2CO3中钠元素的质量为5.3g× 4g NaOH中钠元素的质量为4g× 则原古体混合物中含有钠元素的质量为2.3g+2.3=4.6g 答案:C |
| 点评: | 此题是一道化学计算题,解题的关键是质量守恒定律的巧妙使用,此题难度较大,是一道综合性较强的计算题. |

 阅读快车系列答案
阅读快车系列答案取10g碳酸钙与溶质质量分数为10%的稀盐酸反应,恰好完全反应时间得到溶液的质量为a g;另取10g碳酸钙高温完全分解后,取生成的CaO与上述同浓度的稀盐酸反应,恰好完全反应时得到溶液的质量为b g,则a与b的大小关系为( )
|
| A. | a=b | B. | a>b | C. | a<b | D. | 不能确定 |
形成化学观念是化学学习的任务之.下列说法中错误的是( )
|
| A. | 分子、原子、离子都是构成物质的微粒 |
|
| B. | 物质在水中的溶解过程实质上是原子重新组合的过程 |
|
| C. | 化学变化的过程实质上是原子重新组合的过程 |
|
| D. | 水的三态变化中,分子的能量、运动速率不变 |
人体吸入的O2有2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”.我国科学家尝试用Na2SeO3清除人体内的活性氧,Na2SeO3中的Se(硒)元素的化合价是( )
| A. | +2 | B. | +4 | C. | +6 | D. | ﹣2 |
下列实验方案设计合理的是
| 选项 | 实验名称 | 实验方案 |
| A | 检验某固体物质中是否含有碳酸盐 | 取少量样品于试管中,滴加足量的稀盐酸,看到有气泡产生,则该固体物质中含有碳酸盐 |
| B | 检验集气瓶中是否集满二氧化碳 | 将燃着的木条伸入集气瓶中燃着的木条熄灭集气瓶中已集满二氧化碳 |
| C | 除去二氧化碳中混有的一氧化碳 | 将混合气体通过足量的澄清石灰水,澄清石灰水变浑浊,则得到一氧化碳 |
| D | 鉴别碳酸钠和碳酸钙固体 | 分别取少量样品于试管中,依次滴加足量水,振荡试管,固体溶解的是碳酸钠,无明显变化的是碳酸钙。 |
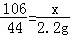
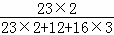 ×100%=2.3g;
×100%=2.3g;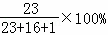 =2.3g
=2.3g 中含碳元素 克,氢元素 克。
中含碳元素 克,氢元素 克。
 方法制备并收集干燥的氧气.
方法制备并收集干燥的氧气. 2Fe+3H2O;其中D1、D2、D3为三个浓硫酸洗气瓶)
2Fe+3H2O;其中D1、D2、D3为三个浓硫酸洗气瓶) 含有(
含有(  )
)