题目内容
4.含相同氧原子数SO2和SO3的质量比为( )| A. | 4:5 | B. | 5:4 | C. | 6:5 | D. | 5:6 |
分析 1个SO2和SO3分子分别含有2个氧原子、3个氧原子,则含相同氧原子数SO2和SO3的分子个数比为3:2,据此进行分析解答.
解答 解:1个SO2和SO3分子分别含有2个氧原子、3个氧原子,则含相同氧原子数SO2和SO3的分子个数比为3:2,则含相同氧原子数SO2和SO3的质量比为(3×64):(2×80)=6:5.
故选:C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
15.如图为四种粒子的结构示意图,以下对相关粒子的描述不正确的是( )
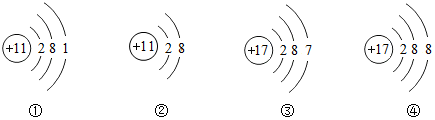

| A. | ②④具有相对稳定结构 | B. | ①②属于同种元素 | ||
| C. | ②④形成的化合物为NaCl | D. | ①③都容易失去电子 |
19.对下列事实的解释,不合理的是( )
| A | 酒香不怕巷子深 | 分子是在不断的运动的 |
| B | 氧气经压缩储存在钢瓶中 | 压强增大,分子之间的间隔变小 |
| C | 干冰升华为二氧化碳气体 | 状态变化,分子大小随之变化 |
| D | 蔗糖在热水中溶解更快 | 温度越高,分子运动速率越大 |
| A. | A | B. | B | C. | C | D. | D |
14.某同学的实验报告中,有以下实验数据,其中合理的是( )
| A. | 用托盘天平称得11.9g面粉 | B. | 用100mL量筒量取2mL硫酸 | ||
| C. | 用量筒量取到4.16mL盐酸 | D. | 用托盘天平称得8.36g铁粉 |
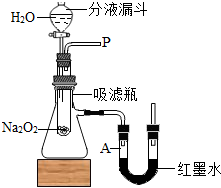 某化学兴趣小组的同学,利用如图装置和药品进行探究.他们设计的探究过程如下:
某化学兴趣小组的同学,利用如图装置和药品进行探究.他们设计的探究过程如下: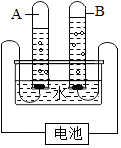 如图为水通电分解的实验装置图,据图分析:
如图为水通电分解的实验装置图,据图分析: