题目内容
18.俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,下表为元素周期表的部分元素的相关信息,利用下表回答相关问题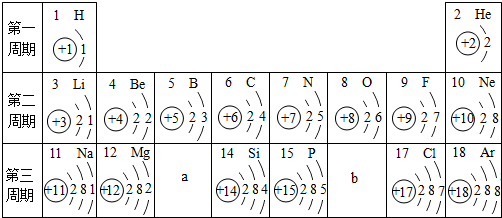
(1)上图中a表示的元素在化学反应中易失去(填“得到”或“失去”)电子变成离子;其离子结构示意图为
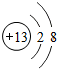 ;
;(2)b表示的元素属于非金属(填“金属”或“非金属”),该元素在氧气中燃烧的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(3)上表中第二、三周期元素最外层电子数的变化规律是从左到右随着核电荷数的依次递增最外层电子数依次增多.
分析 (1)根据a的位置确定元素名称,根据其最外层电子数来确定得失电子情况;
(2)根据元素b的位置确定元素名称,并书写化学方程式;
(3)根据表中各元素最外层电子数的特点分析规律.
解答 解:(1)a处是铝原子,其原子最外层电子数为3,所以在化学反应中易失去最外层的3个电子,而形成铝离子;故填:失去;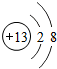 ;
;
(2)b是硫元素,属于非金属元素,硫与氧气在点燃的条件下反应生成二氧化硫,故填:非金属;S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(3)观察表中第二、三周期各元素最外层电子数的变化可以看出最外层电子数从左到右由1递增到8.故填:从左到右随着核电荷数的依次递增最外层电子数依次增多.
点评 本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.

练习册系列答案
相关题目
3.(1)如图I是利用排水法收集的某无色气体.请据此回答该气体应具有的物理性质(色态味除外)密度大于空气.
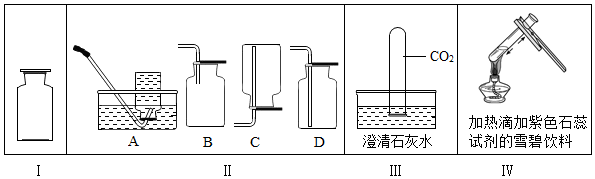
(2)请你用学过的知识进行探究,确定图I无色气体的成分.
(3)如图Ⅱ装置所示,CO2气体的收集方法正确的是D.
(4)如图Ⅲ所示,将收集到的一个充满纯净的二氧化碳气体的试管倒置于澄清的石灰水中,同时轻轻震荡,可观察到的现象是:①溶液变浑浊②试管内液面上升.
(5)如图Ⅳ所示,该实验的现象是溶液由红色变为紫色,出现此现象的原因碳酸不稳定,加热会分解,酸性消失.

(2)请你用学过的知识进行探究,确定图I无色气体的成分.
| 假设(猜想) | 验证操作 | 可能看到的现象 | 结论 |
| 氧气 | 将带火星的木条伸进集气瓶内 | 木条复燃 | 为猜想气体 |
(4)如图Ⅲ所示,将收集到的一个充满纯净的二氧化碳气体的试管倒置于澄清的石灰水中,同时轻轻震荡,可观察到的现象是:①溶液变浑浊②试管内液面上升.
(5)如图Ⅳ所示,该实验的现象是溶液由红色变为紫色,出现此现象的原因碳酸不稳定,加热会分解,酸性消失.
13.原子是构成物质的基本粒子.下列有关原子的叙述错误的是( )
| A. | 原子在化学变化中不能够再分 | B. | 原子质量主要集中在原子核上 | ||
| C. | 原子的质子数等于核电荷数 | D. | 原子的体积比分子小 |
3.下列做法中正确的是( )
| A. | 蒸发溶液时,在蒸发皿下垫石棉网 | |
| B. | 点燃可燃性气体前都必须验纯 | |
| C. | 用湿润的pH试纸粗略测定稀醋酸的pH | |
| D. | 用托盘天平称量时,左盘放砝码右盘放药品 |
10.有X、Y、Z三种金属,它们之间能够发生如下反应:Y+X(NO3)2=X+Y(NO3)2,X+Z(NO3)2=Z+X(NO3)2.问:X、Y、Z三种金属的活动性由强到弱的顺序是( )
| A. | Y>X>Z | B. | X<Y<Z | C. | Z>Y=X | D. | X>Z>Y |
7.将氢氧化钠溶液加入到下列物质的溶液中,可以得到蓝色沉淀的是( )
| A. | K2SO4 | B. | FeC13 | C. | CuSO4 | D. | KNO3 |
8.下列化学方程式的书写正确的是( )
| A. | HCl+Fe2O3→H2O+FeCl3 | B. | Ca(OH)2+H2SO4→CaSO4+2H2O | ||
| C. | 3CO+Fe2O3→2Fe+3CO2 | D. | 2NaOH+SO2→Na2SO4+H2O |
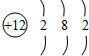 ,该元素原子核内有12个质子,最外电子层上有2个电子.
,该元素原子核内有12个质子,最外电子层上有2个电子.