题目内容
5.向一定质量的FeSO4和CuSO4的混合入溶液中加入一定质量锌粉,充分反应后过滤,得滤液M和滤渣N,向滤渣N中加入稀盐酸,有气泡产生,根据实验现象分析判断下列说法,正确的是( )| A. | 滤液M中一定存在Fe2+ | B. | 滤液M的颜色呈蓝色 | ||
| C. | 滤渣N的质量大于加入锌粉的质量 | D. | 滤渣N中一定含有Fe和Cu |
分析 根据在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来进行分析.
解答 解:在金属活动性顺序中,铜、锌、铁的活动性顺序为:锌>铁>铜,所以向FeSO4和CuSO4的混合溶液中加入一些锌粉,锌先与硫酸铜的反应生成了硫酸锌和铜,当硫酸铜完全反应后,锌再与硫酸亚铁的反应,生成硫酸锌和铁,充分反应后过滤,得滤液M和滤渣N,向滤渣N中加入稀盐酸,有气泡产生,说明了滤渣中一定有铁、铜,可能有锌,溶液中的CuSO4完全发生了反应,所以
A、当滤渣中含有锌时,滤液M中不存在Fe2+,故A错误;
B、由上述分析可知,溶液中不存在CuSO4,滤液M的颜色不会呈蓝色的,故B错误;
C、由化学方程式可知,每65份质量的锌会置换出64份质量的铜或56份质量的铁,锌置换出铜或铁都会使固体的质量减小,所以滤渣N的质量小于加入锌粉的质量,故C错误;
D、由上述分析可知,滤渣N中一定含有Fe和Cu,故D正确.
故选:D.
点评 本题主要考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行解答.

练习册系列答案
相关题目
20.实验室用双氧水制取氧气并进行性质实验,下列操作错误的是( )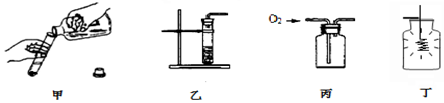

| A. | 甲:加双氧水 | B. | 乙:产生O2 | C. | 丙:收集O2 | D. | 丁:铁丝燃烧 |
10.元素周期表是学习化学的重要依据,如图是元素周期表的一部分,按表格提供的信息判断错误的是( )
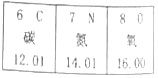

| A. | 碳、氮、氧三种元素都属于非金属元素 | |
| B. | 氧原子的核内中子数是8 | |
| C. | 不同元素之间最本质的区别是最外层电子数不同 | |
| D. | 碳原子的相对原子质量是12.01 |
14.在日常生活中,下列说法不正确的是( )
| A. | 冬天室内用煤炉取暖,为防止煤气中毒,在煤炉上放一盆水 | |
| B. | 包装食品的聚乙烯塑料袋可用加热的方法封口 | |
| C. | 用醋可以洗净铝制品的污垢,还可除去暖壶、水壶中的水垢 | |
| D. | 图书档案着火,最好用液态二氧化碳灭火器灭火 |
15.关于碳单质及其化合物,以下说法错误的是( )
| A. | 金刚石和石墨都是由原子直接构成的 | |
| B. | 碳和一氧化碳都具有可燃性和还原性 | |
| C. | 二氧化碳和一氧化碳能相互转化 | |
| D. | 二氧化碳和一氧化碳均有毒 |
 B.
B. 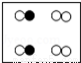 C.
C. 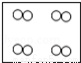 D.
D. 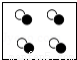
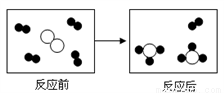
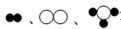 分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )
分别表示X、Y、Z三种不同的气体分子,其在一定条件下的变化如图所示,通过图示得出的下列结论中不正确的是( )