题目内容
根据图中化合物与单质的相互转化关系回答问题.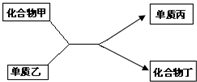
(1)此反应的类型是 ;
(2)①若丁的溶液变为浅绿色,丙为红色固体,乙是 ;
②若常温下甲是固体,丁为无色液体,乙是 ;
(3)写出甲不同于(2)中化合物甲的物质类型的化学方程式 .

(1)此反应的类型是
(2)①若丁的溶液变为浅绿色,丙为红色固体,乙是
②若常温下甲是固体,丁为无色液体,乙是
(3)写出甲不同于(2)中化合物甲的物质类型的化学方程式
考点:物质的鉴别、推断,金属的化学性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式,氢气的化学性质与燃烧实验
专题:常见物质的推断题
分析:运用寻找突破口法和概念辨析法解题,利用置换反应的特征“单+化=单+化”,结合铁盐的溶液为浅绿色、铜为红色金属以及金属与稀酸反应制取氢气进行分析解答.
解答:解:(1)由于该反应的反应物和生成物都是一种单质和一种化合物,所以该反应是置换反应;
(2)①根据信息可知发生的反应是置换反应,因含Fe2+的溶液为浅绿色,铜为红色固体,则此反应为铁与铜盐溶液的置换反应,即硫酸铜溶液与铁反应生成硫酸亚铁与铜,化学方程式是:Fe+CuSO4=Cu+FeSO4,所以单质乙为:Fe;
②在常温下,若乙是液态水,所以该反应是氢气还原金属氧化物生成金属单质和水,所以乙是氢气;
(3)若丙为氢气,锌、铁等排在氢以前的金属可以置换出酸中的氢,所以单质乙为锌、铁等金属,化合物甲是稀硫酸或盐酸,所以可以用Fe+2HCl=FeCl2+H2↑表示该过程.
故答案为:(1)置换反应;
(2)铁,氢气;
(3)Fe+2HCl=FeCl2+H2↑.
(2)①根据信息可知发生的反应是置换反应,因含Fe2+的溶液为浅绿色,铜为红色固体,则此反应为铁与铜盐溶液的置换反应,即硫酸铜溶液与铁反应生成硫酸亚铁与铜,化学方程式是:Fe+CuSO4=Cu+FeSO4,所以单质乙为:Fe;
②在常温下,若乙是液态水,所以该反应是氢气还原金属氧化物生成金属单质和水,所以乙是氢气;
(3)若丙为氢气,锌、铁等排在氢以前的金属可以置换出酸中的氢,所以单质乙为锌、铁等金属,化合物甲是稀硫酸或盐酸,所以可以用Fe+2HCl=FeCl2+H2↑表示该过程.
故答案为:(1)置换反应;
(2)铁,氢气;
(3)Fe+2HCl=FeCl2+H2↑.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学方程式符合题意,且书写正确的是( )
A、用点燃的方法除去CO2中少量的CO:2CO+O2
| ||||
| B、熟石灰和盐酸反应:CaO+2HCl═CaCl2+H2O | ||||
| C、洗去试管壁上附着的铜:Cu+H2SO4═CuSO4+H2↑ | ||||
| D、铁和稀盐酸反应:Fe+2HCl═FeCl2+H2↑ |
60℃时硝酸钾的溶解度为110克.60℃时将60.0克硝酸钾放入50.0克中,充分溶解后,所得溶液的质量百分比浓度为( )
| A、54.6% | B、52.4% |
| C、50% | D、60% |
下列每组物质的名称、俗称、化学式三者不能表示同一种物质的是( )
| A、氯化钠、食盐、NaCl |
| B、氯化氢、盐酸、HCl |
| C、硫酸铜晶体、纯碱晶体、CuSO4?5H2O |
| D、氢氧化钙、熟石灰、Ca(OH)2 |
 小强设计了如图所示装置进行趣味实验
小强设计了如图所示装置进行趣味实验  甲、乙、丙是初中化学常见物质,它们之间转化关系如图所示(部分反应物质和反应条件已略去):
甲、乙、丙是初中化学常见物质,它们之间转化关系如图所示(部分反应物质和反应条件已略去):