题目内容
3.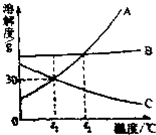 如图是A、B、C三种物质的溶解度曲线.看图回答问题:
如图是A、B、C三种物质的溶解度曲线.看图回答问题:(1)在t2℃时,A、B两种物质的溶解度相同.
(2)在t1℃时,将40gA物质放入100g水中充分搅拌,所得溶液的质量分数是23.1%(计算结果精确到0.1%).若将C的接近饱和的溶液转变为饱和溶液,可用升高温度,蒸发溶液和加入C的固体方法.
(3)在t2℃,将一定质量A物质的饱和溶液降温到t1℃,该过程中没有发生变化的是②(填序号,A的晶体物结晶水).
①溶质的质量 ②溶剂的质量 ③溶液的质量 ④溶质的质量分数
(4)在t2℃,将相同质量的A、B、C三种物质的饱和溶液降温到t1℃,此时三种溶液的溶质的质量分数大小顺序是B>A>C.
分析 (1)根据物质的溶解度曲线可以判断物质的溶解度大小;
(2)饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
饱和溶液和不饱和溶液之间可以相互转化;
(3)温度变化时,溶剂质量不变;
(4)根据物质的溶解度曲线可以判断随着温度的变化,溶质质量分数变化的情况.
解答 解:(1)在t2℃时,A、B两种物质的溶解度相同.
故填:t2.
(2)在t1℃时,A的溶解度是30g,将40gA物质放入100g水中充分搅拌,能够溶解30g,所得溶液的质量分数=$\frac{30g}{100g+30g}$×100%=23.1%;
若将C的接近饱和的溶液转变为饱和溶液,可用升高温度,蒸发溶液和加入C的固体等方法.
故填:23.1%;升高温度;加入C的固体.
(3)在t2℃,将一定质量A物质的饱和溶液降温到t1℃,该过程中,
①溶质的质量减小;
②溶剂的质量不变;
③溶液的质量减小;
④溶质的质量分数减小.
故填:②.
(4)在t2℃,将相同质量的A、B、C三种物质的饱和溶液降温到t1℃时,A和B仍然是饱和溶液,由于B的溶解度大于A的溶解度,因此B的质量分数大于A的质量分数;
因为A在t1℃时溶解度大于C在t2℃时的溶解度,因此降温到t1℃时,A的质量分数大于C的质量分数,此时三种溶液的溶质的质量分数大小顺序是B>A>C.
故填:B>A>C.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
14.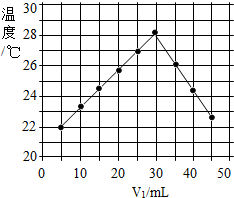 将V1mL3.65% HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,溶液密度均看成1g/mL).下列叙述正确的是( )
将V1mL3.65% HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,溶液密度均看成1g/mL).下列叙述正确的是( )
 将V1mL3.65% HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,溶液密度均看成1g/mL).下列叙述正确的是( )
将V1mL3.65% HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,溶液密度均看成1g/mL).下列叙述正确的是( )| A. | 做该实验时环境温度为22℃ | |
| B. | 该实验表明溶液的pH先升高后下降 | |
| C. | NaOH溶液中溶质质量分数约为6% | |
| D. | 该实验表明有水生成的反应都是放热反应 |
11.下列反应属于复分解反应的是( )
| A. |  | B. |  | ||
| C. | 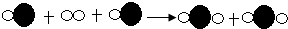 | D. | 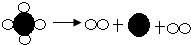 |
8.下列物质的转变,不能由一步反应实现的是( )
| A. | SO3→H2SO4 | B. | Ca(OH)2→NaOH | C. | CuO→Cu(OH)2 | D. | CaCl2→CaCO3 |
15.下列物质在敞口容器中放置一段时间后,因发生化学变化而使其质量增大的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠固体 | D. | 石灰水 |
13.如图所示实验操作不正确的是( )
| A. | 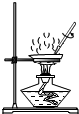 蒸发 | B. |  取用固体粉末 | C. | 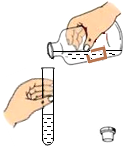 取用液体 | D. | 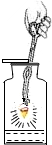 铁丝在O2中燃烧 |
 2015年4月6日18时福建漳州古雷化工厂,盛有二甲苯的储油罐漏油着火,附近三个储油罐也相继被引爆炸,7日16时大火被扑灭.17时40分油罐又死灰复燃,再次被扑灭.火场上空黑烟密布,气味呛人.
2015年4月6日18时福建漳州古雷化工厂,盛有二甲苯的储油罐漏油着火,附近三个储油罐也相继被引爆炸,7日16时大火被扑灭.17时40分油罐又死灰复燃,再次被扑灭.火场上空黑烟密布,气味呛人. 纯碱是一种重要的化工基本原料,工业纯碱中往往会含有少量氯化钠杂质.为测定工业纯碱中碳酸钠的质量分数,某学生设计了如图所示的实验装置:
纯碱是一种重要的化工基本原料,工业纯碱中往往会含有少量氯化钠杂质.为测定工业纯碱中碳酸钠的质量分数,某学生设计了如图所示的实验装置: