题目内容
9.某微粒的结构示意图为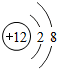 ,表示一种阳离子,它的第二层上有8的电子,这种阳离子是由于在化学反应里该原子丢失2个电子后形成的.
,表示一种阳离子,它的第二层上有8的电子,这种阳离子是由于在化学反应里该原子丢失2个电子后形成的.
分析 根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;粒子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数;若粒子的最外层电子数为8(氦为2个),属于相对稳定结构进行分析.
解答 解:通过分析可知,该微粒表示一种阳离子,它的第二层上有8个电子,质子数=12,核外电子数=10,所以这种阳离子是由于在化学反应里该原子丢失2个电子后形成的.
故答案为:8,2.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
相关题目
19.下列实验现象或结论的描述中错误的是( )
| A. | 碘易溶于水 | |
| B. | 高锰酸钾几乎不溶于汽油 | |
| C. | 乙醇能与水互溶 | |
| D. | 水和植物油混合后用力振荡可形成乳浊液 |
14.下面制取氧气的方法中,从物质变化的角度分析,有一种方法与其他三种方法不同的是( )
| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | |
| B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | |
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| D. | 在一定条件下将空气液化,再将液态空气气化分离,得到氧气 |
1.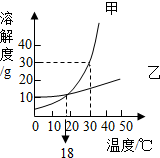 下列对如图所示的溶解度曲线图分析正确的是( )
下列对如图所示的溶解度曲线图分析正确的是( )
 下列对如图所示的溶解度曲线图分析正确的是( )
下列对如图所示的溶解度曲线图分析正确的是( )| A. | 30℃时,甲的溶解度小于乙的溶解度 | |
| B. | 0~30℃时,乙物质溶解度随温度变化比甲大 | |
| C. | 18℃时,甲、乙两物质的溶解度相等 | |
| D. | 甲物质的溶解度大于乙物质的溶解度 |
18.t℃时,18克水溶解2克M物质(不含结晶水),则此溶液溶质的质量分数是( )
| A. | 20% | B. | 11.11% | C. | 10% | D. | 12.50% |
19.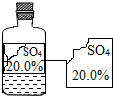 可园学校化学兴趣小组的同学在实验室发现有一瓶无色溶液,由于保管不当,标签残缺不全.下列分析与判断不正确的是( )
可园学校化学兴趣小组的同学在实验室发现有一瓶无色溶液,由于保管不当,标签残缺不全.下列分析与判断不正确的是( )
 可园学校化学兴趣小组的同学在实验室发现有一瓶无色溶液,由于保管不当,标签残缺不全.下列分析与判断不正确的是( )
可园学校化学兴趣小组的同学在实验室发现有一瓶无色溶液,由于保管不当,标签残缺不全.下列分析与判断不正确的是( )| A. | 这瓶溶液的PH值一定为7 | B. | 这瓶溶液不可能是硫酸铜溶液 | ||
| C. | 这瓶液体不可能是碱 | D. | 这瓶溶液中不一定含有金属元素 |